Содержание:

Актуальность. В настоящее время отмечено увеличение количества пациентов с циррозом печени (ЦП). Течение заболевания негативно сказывается на качестве жизни и трудоспособности. Наряду с возросшим количеством случаев вирус-ассоциированного ЦП остается значительной доля больных с алкогольной и аутоиммунной этиологией заболевания. Повышение давления в системе воротной вены (ВВ) сопряжено с развитием ряда жизнеугрожающих осложнений. Портальная гипертензия (ПГ) приводит к варикозной трансформации вен эзофаго-кардиального перехода. Развитие пищеводно-желудочного варикоза наблюдается у подавляющего количества пациентов с ЦП (до 98 %) [1]. Пищеводно-желудочная геморрагия является ведущей причиной смерти у таких больных. При первом же эпизоде кровотечения погибает более половины из них, при второй и третьей геморрагии – до 80 % [2]. В свою очередь, течение внутрипеченочной ПГ в ряде случаев сопряжено и с возможностью развития печеночной энцефалопатии (ПЭ) и гепаторенального синдрома (ГРС) на фоне печеночно-клеточной недостаточности [3].
В настоящее время эффективным и малотравматичным методом лечения и профилактики осложнений ПГ считается операция трансъюгулярного внутрипеченочного портосистемного шунтирования (TIPS/ТИПС) [4]. В клинике РостГМУ в 2007–2017 гг. этому вмешательству подверглись 224 больных. Непосредственный хирургический успех при этой операции достигает 96 %. Отдельную проблему представляют тромбозы шунта при операции TIPS/ТИПС и повторные эндоваскулярные вмешательства. Ниже приведен клинический случай успешной повторной операции.
Пациентка П., 66 лет, поступила в хирургическое отделение клиники РостГМУ в марте 2016 г. Диагноз: аутоиммунный ЦП, портальная гипертензия, пищеводно-желудочный варикоз 3 степени. Первым проявлением заболевания стало пищеводное кровотечение в 2009 г., остановленное комплексом компрессионно-медикаментозных мероприятий. Степень фиброза при эластометрии печени составляла 23,4kPa (F4). С декабря 2014 г., после установления аутоиммунного генеза ЦП в комплекс лечебных мер добавлены кортикостероиды, позволившие в течение 6 месяцев добиться нормализации активности трансаминаз. В 2009–2016 гг. отмечено 3 эпизода варикозной геморрагии. Неоднократно выполнялось эндоскопическое лигирование пищеводных вариксов (рис.1).
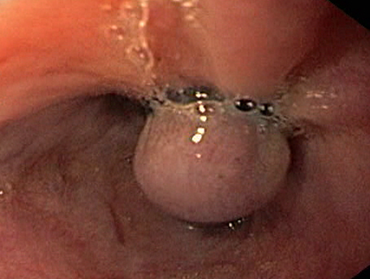
Рис. 1. Эндоскопическое лигирование пищеводных вариксов
В течение месяца, перед операцией, проводилась медикаментозная адаптирующая портальная декомпрессия препаратами пропронолол 10 мг 2 раза в сутки под контролем системного артериального давления и октреотид 100 мкг п/к 1 раз в сутки. Проведенная терапия позволила добиться некоторого снижения давления в системе воротной вены, что подтверждено уменьшением размеров селезенки и рядом других признаков, представленных в таблице.
Признаки снижения давления в системе воротной вены
После мед. лечения
Размер селезенки во фронтальной полоскости при УЗИ, мм.
Диаметр селезеночной вены, мм
Максимальная линейная скорость кровотока по ВВ, см/сек
Показанием к проведению операции TIPS/ТИПС явилась осложнение ПГ, наличие пищеводных вариксов 3 степени с признаками угрозы разрыва. В апреле 2016 г. выполнена операция TIPS/ТИПС, дополненная эмболизацией левой желудочной вены (ЛЖВ). ЛЖВ эмболизирована двумя спиралями Gianturco (рис. 2).
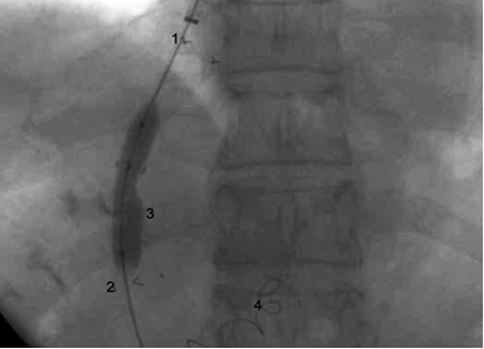
Рис.2. Интраоперационная ангиограмма, цифрами обозначены:
1. Печеночная вена; 2. Воротная вена; 3. Баллонная постдилятация стента, установленного в портосистемном канале; 4. Спирали Gianturco в левой желудочной вене
Интраоперационная манометрия выявила давление в ВВ 39 мм рт. ст. до и 13 мм рт. ст. после шунтирования, в правой печеночной вене до шунтирования 5 мм рт. ст., после -7 мм рт. ст. Таким образом, портосистемный градиент давления (ПСГД), составил до шунтирования 34 мм рт. ст., после – 6 мм рт. ст. Установлен стент-графт между правой печеночной и правой браншей воротной вены длиной 80 мм с шириной просвета 10 мм частично покрытый. Послеоперационный период протекал без осложнений. Коррекция гипераммониемии проводилась препаратами лактулозы, рифаксимина, орнитин-аспартата [5]. С целью профилактики тромбоза шунта назначены дезагреганты (ацетилсалициловая кислота 100 мг 1 раз в сутки) и антикоагулянты (энокссапарин 40 мг/сутки п/к 1 раз в день).
Отмечено уменьшение размеров селезенки до 9 см во фронтальной плоскости (по данным УЗИ).
Ухудшение состояния отмечено в ноябре 2016 г. – рецидив пищеводного кровотечения. Гемостаз достигнут комплексом компрессионно-медикаментозных мероприятий (гемостатическая терапия, установка зонда-обтуратора Блэкмора). Установлен тромбоз шунта, основываясь на отсутствии кровотока при доплерометрии сосудов печени.
13.12.16 г. в РостГМУ выполнена повторная операция портосистемного шунтирования реTIPS/ТИПС параллельной методикой (рис. 3).
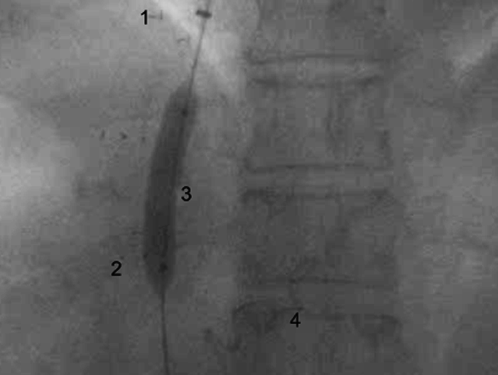
Рис.3. Формирование внутрипеченочного канала параллельной методикой, цифрами обозначены: 1.Проксимальный конец стента, установленный в печеночной вене (04.2016 г.);
2. Дистальный конец стента, установленный в воротной вене (04.2016 г.); 3.Формирование нового канала перед установкой стента параллельной методикой (балонная дилатация);
4. Спираль Gianturco, установленная в левую желудочную вену (04.2016 г.)
Выбор параллельной методики операции основывался на высокой вероятности возникновения тромбоэмболических осложнений при формировании канала внутри уже установленного, тромбированного стента.
Пункция воротной вены производилась из устья средней печеночной вены параллельно тромбированному стенту. Имплантирован стент-графт между средней печеночной веной и устьем правой бранши воротной вены длиной 80 мм с шириной просвета 10 мм частично покрытый. При прямой портографии контрастировались пищеводно-желудочные вариксы из бассейна частично реканализованной левой и преимущественно задней желудочных вен (ЗЖВ). Выполнена эмболизация этих вен двумя спиралями Gianturco. Завершающая прямая портография установила ламинарный кровоток по шунту, контрастирование стента без дефектов наполнения и отсутствие ретроградного кровотока по ЛЖВ и ЗЖВ (рис. 4).
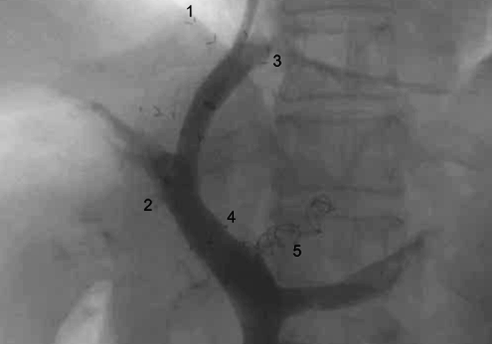
Рис.4. Прямая портография (контроль), цифрами обозначены:
1,2. Проксимальный и дистальные концы тромбированногостента (04.2016 г.);
3,4. Проксимальный и дистальные концы параллельного стента (реТИПС);
5. Спирали Gianturco в левой и правой желудочной вене
Для профилактики тромбоза шунта назначен эноксапарин 40 мг/сутки с переходом через 3 мес. на прием антикоагулянтов peros на фоне постоянного приема дезагрегантов.
В июле 2017 г. – рецидив пищеводной геморрагии, потребовавший мер медикаментозного и эндоскопического гемостаза. Выполнено дуплексное сканирование сосудов гепаторенальной зоны от 02.08.2017 г. между нижней полой веной и воротной веной в правой доле печени лоцируется два портокавальных шунта, при ЦДК кровоток не определен, стенты окклюзированы гетерогенными тромбомассами. Отмечено появление порто-кавальных и спленоренальных анастомозов, не диагностируемых раннее, что явилось спасительным для пациентки. В свою очередь анатомические пути обходного кровотока не обеспечивали достаточного снижения давления в системе ВВ, что подтверждено появлением спленомегалии (156 мм во фронтальной плоскости) с синдромом гиперспленизма (уровень тромбоцитов крови 56х109/л, эритроцитов 2,54х1012/л), и выраженными изменениями венозных структур пищеводно-желудочного перехода. ЭФГДС от 1.08.2017 г. В нижней трети пищевода визуализированы варикозно-расширенные вены до 0,8 см, полнокровные, мелкие эрозии, что соответствует ВРВП 3 ст.
30.08.17 г. поступила в хирургическое отделение РостГМУ.
Для визулизации кровотока по воротной вене произведена мезентерикопортография правым трансрадиальным доступом. В связи с отсутствием кровотока интраоперационно принято решение о выполнении шунтирующего пособия. Пункция воротной вены производилась из устья левой печеночной вены параллельно нефункционирующим шунтам. При прямой портографии контрастированы пищеводно-желудочные вариксы, заполняющиеся из бассейна коротких вен желудка и реканализованной ЗЖВ. Выполнена эмболизация этих вен спиралями Gianturco (рис.5). Затем имплантирован стент-графт между устьем левой печеночной вены и устьем левой бранши воротной вены, длиной 80 мм с шириной просвета 10 мм частично покрытый ПТФЭ. При контрольной прямой портографии кровоток ламинарный, стент контрастируется без дефектов наполнения.
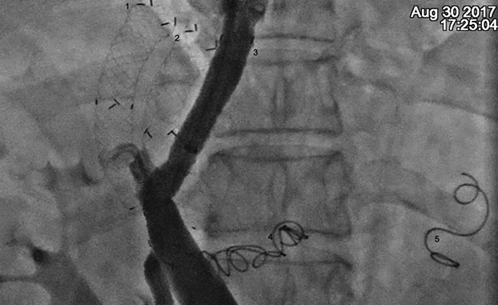
Рис.5. Прямая портография (контроль), цифрами обозначены:
1.Тромбированныйстент, установленный 04.2016 г.; 2. Тромбированный стент, установленный 12.2016 г.; 3. Стент, установленный при оперативном вмешательстве 30.08.2017 г.; 4. Спираль Gianturco, установленная в левую желудочную вену (04.2016 г.);
5. Спираль Gianturco, установленная в заднюю желудочную вену 30.08.2017 г.
С целью выявления коагулопатии, не регистрируемой рутинными методиками исследования системы гемостаза, выполнен анализ тромбодинамики. Проведенное исследование позволило установить наличие агрегационных нарушений форменных элементов крови (тромбоцитов) на фоне общей гипокоагуляции. У пациентки выявлена выраженная спонтанная агрегация тромбоцитов на основании оптической плотности суспензии тромбоцитов. Совместно со специалистами-гемостазиологами, основываясь на результатах агрегатограммы, назначена комплексная терапия антикоагулянтами и дезагрегантами, дозировка которых индивидуально оттитрована исследованием тромбодинамики. Больная осмотрена в декабре 2017 г. – шунт функционирует, что свидетельствует о важности периоперационных мероприятий и необходимости их постоянного моделирования.
Данный клинический случай демонстрирует современные миниинвазивные хирургические возможности осуществления эффективной портальной декомпрессии у пациентов с выраженной хронической печеночной недостаточностью и возможность продления жизни пациентам, находящимся в листе ожидания трансплантации печени. Необходимым является не только проведение оперативного вмешательства, но и динамический контроль функции портосистемного шунта и системы гемостаза в послеоперационном периоде. Применением современных диагностических методик является более информативным по сравнению с рутинными.
Исследование типичных клинических синдромов нарушенного портального кровотока. Изучение основных причин портальной гипертензии. Обзор классификации операций при данном заболевании. Характеристика сущности операций, проводимых при портальной гипертензии.
| Рубрика | Медицина |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 13.05.2016 |
| Размер файла | 20,9 K |

Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
ГБОУ ВПО ОрГМУ МИНЗДРАВА РОССИИ
КАФЕДРА ОПЕРАТИВНОЙ ХИРУРГИИ И КЛИНИЧЕСКОЙ АНАТОМИИ ИМЕНИИ С.С. МИХАЙЛОВА
На тему: «Операции при портальной гипертензии»
Выполнила: Заморева А.С.
Проверил: Фатеев И.Н.
Оренбург, 2016 г.
Причины портальной гипертензии
Классификация операций при портальной гипертензии
Сущность операций, проводимых при портальной гипертензии
Список используемой литературы
Портальная гипертензия — это патологическое состояние, обусловленное повышением давления в системе воротной вены свыше 200 мм вод. ст., что связано с наличием препятствия кровотоку на разных уровнях абдоминальной венозной системы. Типичными клиническими синдромами нарушенного портального кровотока являются увеличение селезёнки, варикозное расширение вен пищевода и желудка с кровотечением из них, асцит, геморрой. У некоторых больных также выявляют гепатомегалию и расширение подкожных вен живота или всего туловища.
Портальная гипертензия наиболее часто наблюдается при циррозе печени. Изменение объемной скорости портального кровотока вызывает значительное повышение портального давления, что способствует интенсивному развитию коллатерального кровообращения. По мере формирования новых анастомозов и открытия существующих соустий дальнейшее нарастание портальной гипертензии замедляется. Развитие коллатералей в большинстве случаев недостаточное, часто приводит к выраженным дистрофическим изменениям внутренних органов.
Причины портальной гипертензии
Этиологические факторы, приводящие к развитию портальной гипертензии, многообразны. Ведущей причиной выступает массивное повреждение печеночной паренхимы вследствие заболеваний печени: острых и хронических гепатитов, цирроза, опухолей печени, паразитарных инфекций. Портальная гипертензия может развиваться при патологии, обусловленной внепеченочным или внутрипеченочным холестазом, вторичном билиарном циррозе печени, первичном билиарном циррозе печени, опухолях холедоха и печеночного желчного протока, желчнокаменной болезни, раке головки поджелудочной железы, интраоперационном повреждении или перевязке желчных протоков. Определенную роль играет токсическое поражение печени при отравлениях гепатотропными ядами.
К развитию портальной гипертензии может приводить тромбоз, врожденная атрезия, опухолевое сдавление или стеноз портальной вены; тромбоз печеночных вен при синдроме Бадда-Киари; повышение давления в правых отделах сердца при рестриктивной кардиомиопатии, констриктивном перикардите. В некоторых случаях развитие портальной гипертензии может быть связано с критическими состояниями при операциях, травмах, обширных ожогах, ДВС-синдроме, сепсисе.
Непосредственными разрешающими факторами, дающими толчок к развитию клинической картины портальной гипертензии, нередко выступают инфекции, желудочно-кишечные кровотечения, массивная терапия транквилизаторами, диуретиками, злоупотребление алкоголем, избыток животных белков в пище.
портальная гипертензия операция кровоток
Классификация операций при портальной гипертензии
Показаниями к оперативному вмешательству при портальной гипертензии являются: кровотечение из варикозно расширенных вен пищевода и желудка, спленомегалия, гиперспленизм и асцит.
Существует классификация операций, выполняемых при портальной гипертензии.
I. По виду выполняемой операции выделяют следующие типы:
1. Межсосудистые анастомозы: Спленоренальный анастомоз; Мезентерикокавальный анастомоз; Прямой портокавальный анастомоз; Перитонеовенозное шунтирование;
2. Паллиативные операции: Перевязка ветвей чревного ствола; Спленэктомия: Органоанастомозы: Пишеводно-кардиальная резекция и гастрэктомия; Операции, дренирующие брюшную полость; Операции при продолжающемся кровотечении из вен пищевода.
II. По времени выполнения выделяют следующие типы операций:
1. Экстренные операции — проводятся на высоте кровотечения при безуспешности его остановки другими методами лечения. Характеризуются высокой послеоперационной летальностью, особенно у пациентов с выраженным нарушением печеночной функции. По данным разных авторов послеоперационная смертность достигает 9-20% при классе цирроза А, 18-37% при классе цирроза В и 60-80% при классе цирроза С.
2. Операции первичной профилактики — проводятся при наличии варикозных вен и отсутствии в анамнезе кровотечения, однако статистически значимого улучшения выживаемости по сравнению с группами пациентов, получивших медикаментозную терапию и эндоскопическое лечение, при этом не отмечено. 3. Операции вторичной профилактики (элективные) — выполняются в ранние сроки после кровотечения и являются наиболее перспективным методом оперативного лечения кровотечений из ВРВ пищевода и желудка при ПГ.
III. В зависимости от механизма действия выделяют две основные группы операций:
1.Направленные на декомпрессию портальной системы — шунтирующие операции.
2. Прекращающие приток крови в ВРВ пищевода и желудка путем разобщения венозных систем воротной и верхней полой вен — разобщающие операции.
Противопоказаниями для оперативного вмешательства при ПГ являются: декомпенсированная портальная гипертензия, наличие активного воспалительного процесса в печени, выраженные проявления печеночно-клеточной недостаточности.
Сущность операций, проводимых при портальной гипертензии
Спленоренальный анастомоз — это вид соустья между системой воротной и нижней полой вены наиболее распространен среди других портакавальных ангиоанастомозов.
Спленоренальный анастомоз впервые был выполнен в 1967 г. Д. Вареном. Метод базируется на создании двух изолированных зон давления в брюшной полости: низкого давления в левой половине брюшной полости (за счет оттока крови из гастроэзофагеальной области через короткие вены желудка и левую желудочно-сальниковую вену в селезенку, а оттуда через анастомоз «конец в бок» с левой печеночной веной в систему нижней полой вены) и высокого давления в правой половине (за счет сохраненного мезентериального венозного притока в воротную вену), что препятствует дальнейшему снижению портальной перфузии и значительно уменьшает вероятность развития послеоперационной энцефалопатии. В дальнейшем были предложены анастомозы между левой желудочной и левой почечными венами, анастомоз «бок в бок» между нижней брыжеечной и нижней полой венами, анастомозы с использованием аутовенозной и синтетических вставок. Расширенная селезеночная вена и лигирование селезеночной артерии.
Портокавальный анастомоз — это анастомоз, который обеспечивает переход крови из воротной вены в системы верхней и нижней полых вен. Парциальное портокавалъное шунтирование осуществляют с помощью анастомозов «бок в бок» и «Н»-типа малого диаметра (8-10 мм), выполняемых с любым сосудом портальной системы, кроме воротной вены. При этом типе операции с одной стороны, обеспечивают декомпрессию портальной системы, достаточную для регрессии варикоза вен и профилактики пищеводно-желудочных кровотечений; с другой — сохраняют редуцированный воротный кровоток для поддержания удовлетворительной функции печени.
Абдоминальный парацентез — при данной операции механически механически асцитическая жидкость из брюшной полости через прокол кожи в области пупка. Специальный клапан позволяет осуществлять процедуру многократно.
Трансъюгулярное внутрипеченочное портосистемное шунтирование заключается в создании искусственного внутрипеченочного канала между печеночной веной и крупным стволом воротной вены и установке в него металлического саморасправляющегося стента. Эта методика позволяет практически всегда остановить кровотечение, в том числе и рефракторное к другим видам терапии. Процедуру выполняют под местной анестезией, ее этапы включают: пункцию яремной вены, проведение катетера в среднюю печеночную вену, пункцию воротной вены (иглой, проведенной по катетеру), расширение пункционного канала баллоном (по установленному через иглу проводнику), постановку стента. Основным недостатком методики является практически неизбежное развитие печеночной энцефалопатии, высокая ее сложность и малая доступность в условиях нашей страны.
Операция М. Д. Пациоры — представляет собой прошивание кровоточащих вен пищевода и кардиального отдела желудка. Из абдоминального доступа выполняется гастротомия, прошивание и перевязка вен дистального отдела пищевода и проксимального отдела желудка. При проведении этого вмешательства ранняя послеоперационная летальность довольно низкая — до 15%. В тоже время отмечается высокая частота рецидивов кровотечения в раннем послеоперационном периоде (10-20%) и в течение последующих 5 лет (45-60%).
Перитонеовенозное шунтирование. На брюшину накладывают кисетный шов, в центре которого делают отверстие и через него вводят заборную трубку в брюшную полость. Под кожей живота и грудной клетки делают туннель до правой ключицы. В туннеле проводят шунт, выполняя дополнительный разрез кожи над ключицей. Выделяют внутреннюю или наружную яремную вену и в нее вводят отводящий катетер.
Оменопариетопексия — создание обходных сосудистых коллатералей путем подшивания большого сальника к передней брюшной стенке.
Операции, способствующие отведению асцитической жидкости — перитонеально-венозное шунтирование (клапаны Левина, Денвера), лимфовенозный анастомоз.
Радикальные операции (удаление опухолей, кист, тромбов, вскрытие абсцессов, обширные резекции печени вместе с опухолью, экстирпация пораженной печени с пересадкой здоровой.
Дренирование брюшной полости. Операция Кальба (1916). В области бедренных треугольников иссекают участки париетальной брюшины и мышц диаметром до 3—4 см. Лапаротомный разрез ушивают наглухо, в результате, асцитическая жидкость всасывается подкожной клетчаткой.
Дренирование брюшной полости. Ронте (отведение жидкости в сосудистое русло). Большую подкожную вену выделяют на протяжении 10—15 см и пересекают, периферический конец ее перевязывают, а центральный заворачивают кверху и вшивают в отверстие брюшины над паховой связкой.
В 1964 г. Уалкер предложил операцию, идея которой состоит в разобщении систем воротной и верхней полой вен путем полного пересечения пищевода или желудка с последующим восстановлением их целостности — трансторакальную пищеводную транссекцию с ручным эзофагоэзофагоанастомозом. При торакотомии достигается хороший доступ к источнику кровотечения и быстрая его остановка, однако из-за травматичности выполнения при этой операции отмечается высокая летальность (30-70%).
Спленэктомия. Хотя спленэктомия как самостоятельная операция ведет к снижению портального давления, однако это практически не влияет на размер варикозных вен и частоту рецидива кровотечений из них и поэтому не оказывает значимого клинического эффекта. В тоже время, удаление селезенки сопровождается ростом летальности, связанной с частым развитием таких послеоперационных осложнений, как внутрибрюшное кровотечение, абсцессы, тромбоз воротной вены, развитие аспленической геморрагической тромбоцитопении. В связи с этим показания к спленэктомии как к самостоятельной операции при ПГ в настоящее время резко сужены. Они ограничиваются тремя ситуациями: 1) сегментарной внепеченочной ПГ, когда болезнь проявляется в основном профузными кровотечениями из варикозных вен желудка вследствие непроходимости селезеночной вены; 2) сосудистой фистулой между селезеночной артерией и селезеночной веной, приводящей к ПГ вследствие перегрузки объемом крови; 3) при инфантилизме у подростков, когда удаление селезенки больших размеров ведет к быстрой нормализации физических параметров организма.
На сегодняшний день проблема портальной гипертензии и ее основных осложнений — кровотечения из варикозно расширенных вен пищевода и желудка, а также риск возникновения летального исхода, являются насущной проблемой современной хирургии.
Для решения этого вопроса оперативная хирургия продолжает разрабатывать новые способы устранения портальной гипертензии с как можно меньшим развитием осложнений и успешно применять современные методы лечения портальной гипертензии.
Список используемой литературы
1. Ерамишанцев А. К. Эволюция хирургического лечения кровотечений из варикозно расширенных вен пищевода и желудка / Ерамишанцев А. К. под ред. В. С. Савельева. — М.: Медиа Медика, 2003. — С. 261-267.
2. Подымова С.Д. Болезни печени / Подымова С.Д. — М.: ОАО «Изд-во «Медицина», 2005. — 768 с.
3. Борисов А. Е., Андреев Г. Н., Земляной В. П. и др. Современные методы хирургической коррекции асцитического синдрома при циррозе печени/ Борисов А. Е., Андреев Г. Н., Земляной В. П. // журн. Политехника, 2000. — 222 с.
4. Любивый Е. Д., Киценко Е. А. Сравнительная оценка результатов портокавальных анастомозов и прошивания варикозно расширенных вен пищевода и желудка у больных циррозом печени и портальной гипертензией/ Любивый Е. Д., Киценко Е. А. // Актуальные проблемы соврем. хирургии: Тез. межд. хирург. конгресса. — М.:2003. — 21 с.
5. Назыров Ф. Г., Акилов Х. А., Мансуров А. А. и др. Опыт лечения кровотечений из варикозного расширения вен пищевода и желудка при циррозе печени / Назыров Ф. Г., Акилов Х. А., Мансуров А. А. // Актуальные проблемы соврем. хирургии: Тез. межд. хирург. конгресса. — М., 2003. — 14 с
Размещено на Allbest.ru
Подобные документы
Этиология портальной гипертензии. Коррекция водно-электролитных нарушений и поддержание сердечно-сосудистой деятельности. Лечение асцита. Степень компенсации активности процесса в печени по Чайлду-Пью. Операции гемодинамической коррекции болезни.
реферат [38,9 K], добавлен 02.05.2015
Классификация портальной гипертензии. Основные причины развития предпеченочной, внутрипеченочной и постпеченочной портальной гипертензии. Повышение сопротивления соответствующего участка сосудистого русла. Нарушение оттока в системе воротной вены.
реферат [29,9 K], добавлен 25.06.2015
Понятие портальной гипертензии как синдрома повышенного давления в системе воротной вены. Симптомы портальной гипертензии, сопутствующие заболевания. Цирроз печени как одна из причин возникновения заболевания, его эпидемиология, классификация и патогенез.
презентация [2,1 M], добавлен 29.03.2015
Формирование коллатерального кровообращения через портокавальные анастамозы при портальной гипертензии. Варикозное расширение вен пищевода (ВРВП) вследствие портальной гипертензии. Эндоскопические и эндоваскулярные методы остановки кровотечения из ВРВП.
реферат [1,1 M], добавлен 06.04.2015
Предпеченочный блок: цирроз печени, кисты и опухоли печени, эхинококкоз, фрожденный фиброз. Осложнение портальной гипертензии: печеночная энцефалопатия, асцит, варикозное расширение вен пищевода, брюшной стенки, прямой кишки. Лечение данного заболевания.
презентация [704,1 K], добавлен 22.03.2016
Хроническое прогрессирующее заболевание печени человека. Значительное уменьшение числа функционирующих гепатоцитов, перестройка структуры паренхимы и сосудистой системы печени с последующим развитием печеночной недостаточности и портальной гипертензии.
презентация [11,1 M], добавлен 28.05.2014
Воспаление желчного пузыря. Главные симптомы при остром холецистите. Рак желчного пузыря и внепеченочных желчных протоков. Синдром портальной гипертензии. Острый отек и кисты поджелудочной железы. Клинические проявления хронического панкреатита.
реферат [43,0 K], добавлен 24.06.2012
Определение симптоматической (вторичной) гипертензии. Распространенность заболевания, классификация, этиология, патогенез. Почечные гипертензии: реноваскулярные, при интерстициальном нефрите, при паренхиматозных поражениях. Заболевания паренхимы почек.
презентация [2,3 M], добавлен 19.05.2012
Изучение причин и методов диагностики полиурии, под которой понимают увеличение суточного диуреза до 3 литров и более. Характеристика синдрома Фанкони, который проявляется генерализованной проксимальной тубулопатией. Диагностика артериальной гипертензии.
реферат [27,1 K], добавлен 01.05.2010
Главные симптомы гипертензии. Ее основные типы и причины. Возможные осложнения артериальной гипертензии. Ретинопатия как уплотнению стенки сосудов внутренней части глаза – сетчатке. Медикаментозное и немедикаментозное лечение артериальной гипертензии.
презентация [165,7 K], добавлен 21.08.2014

Работы в архивах красиво оформлены согласно требованиям ВУЗов и содержат рисунки, диаграммы, формулы и т.д.
PPT, PPTX и PDF-файлы представлены только в архивах.
Рекомендуем скачать работу.
Одним из грозных осложнений цирроза печени является развитие синдрома портальной гипертензии, характеризующегося повышением давления в системе воротной вены.






При декомпенсированной форме портальной гипертензии развиваются варикозное расширение вен пищевода, желудка, спленомегалия и асцит.
Одной из последних новаторских технологий в лечении портальной гипертензии, асцитического синдрома, кровотечения из варикозных вен нижней трети пищевода и желудка, внедренных в отделении рентгенхирургических методов диагностики и лечения ФГБУ «Клиническая больница № 1» явилась эндоваскулярная операция — трансъюгулярное интрапеченочное портокавальное шунтирование (TIPSS).
Данная операция позволяет выполнить эффективную декомпрессию портальной системы, профилактику развития рецидивирующих кровотечений из варикозно расширенных вен пищевода и желудка, асцитический синдром, и значительно улучшает качество жизни пациентов. ТИПС является альтернативой хирургическим методам лечения портальной гипертензии и имеет ряд преимуществ перед достаточно травматичными хирургическими шунтирующими операциями.
Операцию ТИПС часто применяют как поддерживающую, восстанавливающую перед пересадкой печени пациентам с циррозом печени в стадии C. С ростом опыта, развитием рентгенэндоваскулярной хирургии, рефрактерный асцит (асцит неподдающийся медикаментозной терапии) становиться ведущим показанием к ТИПС во многих медицинских клиниках. Если, больному поставлен диагноз рефрактерный асцит, больной имеет плохой прогноз – 50% смертность в течение 12 месяцев без соответствующего лечения. После выполнения ТИПС асцит уменьшается в 58% случаев (при выполнении лапароцентеза эта цифра составляет 19%).
Лучший способ описать ТИПС – объяснить, что значит каждая буква:
Т (трансъюгулярное) – термин обозначающий, что рентгенэндоваскулярный хирург, выполнив местное обезболивание, начинает операцию с пункции иглой яремной вены, расположенной на шее. Через иглу проводится тонкий проводник до момента попадания кончика проводника в печеночную вену. Далее по проводнику проводится специальный катетер.
И (интрапеченочное) – термин обозначающий, что катетер проводится через печеночную вену в саму печень. Затем вводится длинная изогнутая игла.
П (порто-системное) – термин обозначающий, что игла введенная через печеночную вену, проткнув ткань печени, попадет в воротную вену, расположенную так же в самой печени.
C (стентирование или шунтирование (shunt)) – термин обозначающий создание сообщения между печеночной и воротной венами путем имплантации стента.
Стент растягивает печеночную паренхиму создав канал между ветвью воротной и печеночной вены.
После стентирования кровь дренируется из воротной вену с повышенным давлением в печеночную вену со сниженным давлением, что приводит к устранению портальной гипертензии, спаданию расширенных вен пищевода. Давление в воротной вене снижается до нормальных величин, что приводит к резкому улучшению клинического состояния больного.
Для TIPSS существуют строго определенные показания:
- портальная гипертензия;
- острое кровотечение из варикозно расширенных вен пищевода и желудка;
- повторное пищеводно-желудочное кровотечение;
- рефрактерный асцит (асцит неподдающийся медикаментозной терапии);
- печеночный гидроторакс (скопление асцитической жидкости в плевральной полости);
- синдром Бадда-Киари (сдавление нижней полой вены в инфраренальном отделе узлами регенератами).
Клиническую эффективность мы оцениваем по прекращению или уменьшению проявлений портальной гипертензии — прекращение пищеводно-желудочного кровотечения, уменьшение количества асцитической жидкости, спадание варикозно расширенных вен передней брюшной стенки. В послеоперационном периоде больным проводится стандартный курс инфузионной, гемостатической и диуретической терапии.
При необходимости, ТИПС может быть дополнен эндоваскулярной эмболизацией варикозно расширенных вен пищевода и желудка.
В настоящее время в ФГБУ «Клиническая больница №1» оказывается высокоспециализированная медицинская помощь любой сложности у больных с циррозом печени и его осложнений с использованием современного инструментария.
д.м.н., профессор Бояринцев В.В.,
д.м.н., профессор Гибадулин Н.В.,
к.м.н. Закарян Н.В.,
к.м.н. Панков А.С.
Статья добавлена 14 января 2013 г.