Содержание:
 Если быть точными, то острый лимфобластный лейкоз у детей и взрослых характеризуется поражением белых кровяных телец или же лейкоцитов. Особенностью является быстрое распространение болезни на лимфатическую систему, печень или же центральную нервную систему.
Если быть точными, то острый лимфобластный лейкоз у детей и взрослых характеризуется поражением белых кровяных телец или же лейкоцитов. Особенностью является быстрое распространение болезни на лимфатическую систему, печень или же центральную нервную систему.
Говоря «острый», врачи подразумевают быстрое прогрессирование недуга или переход на другие органы или же ткани. В случае когда лечение вообще не наблюдается, то выживаемость равна нулю. Обратите внимание, что заболевание затрагивает незрелые лимфоидные клетки.
Стоит сказать, что многие виды лейкоза лечатся достаточно успешно. Главное – только вовремя начать терапию. Что же касается статистики, то наблюдается недуг у одного пациента на 750 человек. Чаще всего, он поражает мужчин и детей. Таким образом, следует проводить систематические обследования, дабы вовремя выявить влияние и назначить терапевтический процесс.
Основные причины
Точные данные пока выявлены не были. Все же медицине известны основные причины возникновения. Рассмотрим их более подробно:
- Высокие уровни радиации. Даже лучевая терапия способствует развитию лейкоза, особенно если проводится она с химиотерапией.
- Бензол и другие препараты негативно сказываются на здоровье, вызывая подобные симптомы.
- Редкие вирусные инфекции, такие как Т-клеточный лейкоз.
- Достаточно часто имеет значение и наследственный фактор. Конечно, заболевание не передается таким образом, но существуют некоторые синдромы, повышающие риск возникновения.
- Этническая принадлежность. Исследования показывают, что у афроамериканцев лимфобластный лейкоз
 наблюдается гораздо реже.
наблюдается гораздо реже. - Обратите внимание, что мужчины болеют чаще, чем женщины.
- Ряд других причин. На самом деле, теорий достаточно много, однако верить в них довольно сомнительно. Одни говорят про электромагнитное влияние, другие – про краску для волос.
Так как достоверных сведений не имеется, лучше всего вести здоровый образ жизни, а также избегать негативного влияния извне.
Основные симптомы
Если верить практике, то основными признаками являются потеря аппетита, снижается масса тела, а также постоянная усталость. В некоторых случаях наблюдаются лихорадки или же ночная потливость. Это далеко не все:
- Недостаток нормальных клеток крови. В этом случае возникают частые кровотечения, одышка, постоянные инфекции.
- Так как клетки часто накапливаются во внутренних органах, например, в печени или селезенке, то они увеличиваются в размерах. Как результат, живот отекает.
- Увеличение лимфатических узлов также говорит о наличии заболевания. В этом случае поражаются основные ткани.
- Боль в костях и суставах. Патологические клетки также могут накапливаться в суставах или же костях человека.
- Увеличенная в размерах вилочковая железа.
Как проходит лечение
Заметили первые признаки у себя или ребенка? Сразу же направляйтесь к специалисту. Именно он назначит все необходимые анализы по программе. Да, лимфобластный лейкоз достаточно тяжело выявить на ранних стадиях, однако ранняя тревога даст нужные результаты.
Как и всегда, используются химические препараты, которые убивают раковые клетки в крови, снижая распространение патологии.
Возможные прогнозы
Стоит сказать, что некоторые исследования в этой области дали понять, какие особенности человека помогают легче перенести недуг:
- Во-первых, это возраст. Чем моложе пациент, тем шансы на выздоровления будут гораздо больше.
- Низкое число лейкоцитов при постановке диагноза повышает шансы на положительные результаты лечения.
- Выживаемость при Т-клеточном лейкозе гораздо выше, чем при В-клеточном.
- Полная ремиссия – первый успех. У тех пациентов, которые достигли этого на шестой неделе, выздоровление проходит быстрее.
Также имеет значение, насколько же хорошо влияют препараты. Достаточно часто врачи используют термин «ремиссия». Это временные рамки, когда симптомы болезни не наблюдаются. Что же касается ремиссии лейкоза, то показания должны быть в норме, например, уровень лимфобластных клеток не превышает 5%, а количество лейкоцитов ближе к норме.
Минимальная остаточная болезнь – это период, когда обычные исследования не дают положительных результатов. Зато патологии подтверждаются при цитометрии. Стоит сказать, что пациенты, услышавшие данный термин, должны готовиться к рецидиву. Прогнозы не являются достаточно положительными.
Как бы там ни было, а своевременное обращение к профессионалам решает многое. Практика показывает, что современные отечественные больницы достаточно ограничены в своих методах, соответственно, и лечение окажется неэффективным.
Таким образом, следует уделять внимание только настоящим специалистам с богатым опытом работы и качественным оборудованием. Именно они поставят вам точный диагноз и назначат необходимые препараты.
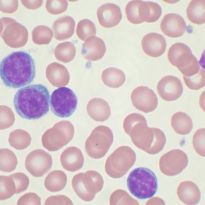
Острый лимфобластный лейкоз у взрослых людей диагностируется намного реже, чем у детей. Наиболее опасный период — это возраст до 2 лет и после 60. Девочки страдают от этой болезни реже мальчиков. Лимфобластная форма недуга является довольно распространенной среди лейкозов и составляет около 80% их общего количества.
Для болезни характерно поражение лимфатических узлов вилочковой железы, костного мозга, внутренних органов. Недуг относят к злокачественным заболеваниям крови, при которых лимфобласты быстро распространяются по кровеносной системе.
Прогноз жизни зависит от ряда факторов, к которым относят возраст, длительность и форму болезни, степень поражения внутренних органов при распространении метастазов.
Особенности заболевания в зависимости от возраста
У взрослых недуг протекает в более тяжелой форме, нежели у детей. К группе риска относят малышей до 7 лет, пожилых людей. Так как болезнь на ранних стадиях имеет скрытую симптоматику, очень сложно определить патологию на начальном этапе.
.jpg)
Сначала у человека появляется анемический синдром, то есть больной становится вялым, начинает быстро уставать. У детей это состояние обычно протекает с потерей аппетита и резким снижением веса.
Развитие лейкоза начинается, когда поражаются клетки костного мозга, нарушается кровообращение и незрелые кровяные тельца постепенно начинают заменять здоровые лейкоциты.
В крови происходит снижение клеток тромбоцитарного, эритроцитарного ряда и уменьшается количество лейкоцитов. У больного начинается малокровие, длительные недуги инфекционного характера, периодические кровотечения.
Так как при появлении болезни очень быстро поражается иммунная система, то ребенок имеет все шансы получить вдобавок инфекционную хворь, поэтому необходимо ограждать его от внешних неблагоприятных факторов.
У взрослых недуг чаще, чем у деток, может заканчиваться неожиданным летальным исходом. Помимо этого, у маленьких больных ниже риск появления рецидива.
Причины болезни
Медициной еще точно не установлены причины возникновения рака. В настоящее время к провоцирующим факторам, повышающим риск появления заболевания, относятся:
- Выкидыш с летальным исходом для плода.
- Инфекционные патологии.
- Перенесение лучевой химиотерапии, влияние ионизирующей радиации.
- Генетическая предрасположенность, присутствие новообразований у других членов семьи.
- Рождение крупного плода более 4 кг.
К группе риска можно отнести детей, матери которых в период беременности неправильно питались или прошли рентгенологическое обследование незадолго до зачатия либо при вынашивании. Также болезни подвержены малыши с некоторыми врожденными патологиями, например, болезнью Дауна или пороком сердца.
Признаки недуга
Симптомы патологии могут заключаться в наличии:

- Интоксикации. Больной испытывает слабость, потерю аппетита и веса, его может беспокоить повышение температуры, рвота.
- Гиперпластического синдрома. Увеличиваются лимфатические узлы, а при прощупывании есть боль в зоне конгломератов.
- Анемии. Кожа при этом становится бледной, слизистые ротовой полости могут кровоточить, возникает тахикардия, геморрагический синдром.
Иногда наблюдаются и сопутствующие признаки недуга. Так, у мальчиков появляется болезненность в зоне яичек, почек. При недостатке тромбоцитов может произойти кровоизлияние в легочную ткань и сетчатку, частые симптомы у детей включают появление сыпи и багровых пятен.
Нередко наблюдается отек зрительного нерва, дыхательная недостаточность.
У ребенка может болеть все тело, он становится плаксивым и перестает двигаться, пытаясь оставаться в том положении, при котором боль менее выражена. Такие дети часто просятся на руки.
У взрослых симптоматика идентична, ее выраженность может меняться в зависимости от индивидуальных особенностей протекания патологии.
Осложнения болезни
Если своевременно не провести лечение, то могут возникнуть следующие осложнения:
.jpg)
- Паралич нерва на лице.
- Нарушение зрения, вплоть до полной слепоты.
- Постоянные мигрени, не прекращающиеся даже при приеме соответствующих препаратов.
Если больному своевременно не оказать медицинскую помощь, то онкологическое заболевание приводит к летальному исходу, так как через кровь стремительно распространяется по всему организму, поражая лимфоузлы, селезенку и вилочковую железу.
Фазы развития патологии
Недуг может иметь 4 степени сложности. Их разделяют по имеющимся симптомам и процессам, происходящим в организме:
- Начальная фаза. Длительность ее от 1 до 3 месяцев. В этот период болезнь только начинается. Пациент ощущает вялость, быструю утомляемость, снижение аппетита. Кожные покровы становятся бледными. Локализация боли может наблюдаться в костной структуре, в зоне головы и живота.
- Фаза разгара. Симптоматика становится ярче. Наблюдаются выраженные признаки анемии и интоксикации, увеличиваются лимфоузлы. Больного может беспокоить тошнота, рвотные позывы, кровотечения, преимущественно носовые.
- Ремиссия. Все симптомы исчезают, создавая на короткий период ложную картину исчезновения патологии.
- Терминальный период. Состояние пациента стремительно ухудшается и может окончиться летальным исходом.
Диагностика
Врач проводит сбор анамнеза и узнает характер симптоматики пациента. Далее больного направляют на сдачу материала для соответствующих анализов и прохождение необходимых обследований, чтобы подтвердить или опровергнуть диагноз.
.jpg)
- Биохимический и общий анализы крови нужны для того, чтобы определить уровень лейкоцитов, эритроцитов, гемоглобина, тромбоцитов. Эти данные могут показать степень поражения печени и почек. Помимо этого, в крови можно обнаружить метамиелоциты и миелоциты.
- Рентгенографию грудной клетки.
- УЗИ, которое помогает выявить увеличение лимфатических узлов и пронаблюдать изменения внутренних органов.
- Миелограмма. Манипуляции выполняются в три этапа. Первый заключается во взятии материала для морфологической цитологии, чтобы распознать гиперклеточность костного мозга и инфильтрацию бластных клеток. После делают цитохимический анализ, а последним выполняется иммунофенотипирование для определения типа клеток.
- Пункция спинного мозга. Помогает определить рак, степень и присутствие поражения ЦНС.
Помимо этого, как дополнительные средства диагностики могут назначаться анализы мочи, ЭКГ или ЭХО-КГ.
Лечение патологии
При остром лимфобластном лейкозе основными мерами являются:
- Химиотерапия, которая проводится в несколько этапов.
- Лучевая терапия.
- Иммунотерапия.
- Пересадка.
Химиотерапия
Прием специальных препаратов разделяют на следующие этапы лечения:
- Период индукции. Может составлять нескольких недель или месяцев. Обычно назначают цитостатики, которые способствуют разрушению лейкемических клеток и восстанавливают нормальное кроветворение. Из препаратов наиболее популярны Винкристин, Глюкокортикостероиды, Антрациклин, Аспарагиназ. В большинстве случаев эта терапия позволяет добиться ремиссии.
- Период консолидации. Может продолжаться месяцы. В это время пациенту назначают специальные препараты, которые окончательно убирают патогенные клетки. Чаще всего используют Метотрексат, Винкристин, Преднизолон, Аспарагиназ, Цитарабин.
- Период ремиссии, поддерживающей терапии. Обычно этот этап самый длительный, он может составлять несколько лет. Терапия заключается в поддержании организма для предотвращения рецидива. Из препаратов обычно назначают Метотрексат, 6-меркаптопурин.
Смена препаратов может производиться только лечащим врачом, это случается при непереносимости либо индивидуальных реакциях организма. Помимо этого, в процессе лечения могут назначаться антибиотики и поливитамины.
Чтобы следить за эффективностью терапии, часто после назначения курса препаратов (через 1-2 недели) проводится биопсия костного мозга. Если бластные клетки уменьшаются наполовину или больше, это указывает на достаточно хороший результат лечения. Дальнейшие взятие материала происходит через месяц после лечения.
Спустя определенное время после достижения результата препараты оставляют для закрепления эффекта, но их дозы уменьшают в два раза.
Иные методы лечения
В случае если болезнь поражает маленького ребенка, наряду с химиотерапией обязательно назначается иммунотерапия. Клинические рекомендации включают введение специальных вакцин по возрасту, необходимых для укрепления иммунитета БЦЖ. Вводят интерфероны и иммунные лимфоциты.
У детей лечение может проводиться наряду с пересадкой костного мозга, которая даёт очень хороший результат.
Лучевая терапия заключается в применении рентгеновского излучения для удаления раковых клеток и остановки их роста. Такая процедура может быть как внешней, так и внутренней.

В первом случае аппаратом производится фокусировка излучения в зоне новообразования. При внутренней лучевой терапии применяют препараты радиоактивного действия, которые герметично упакованы в капсулы, катетеры. Их необходимо разместить в месте новообразования.
Внешняя терапия чаще всего применяется при лечении взрослых с острым лимфобластным лейкозом, когда существует тенденция к распространению патогенных клеток в спинной мозг.
Осложнения при лечении
Длительный период приема таких препаратов, как Винкристин, может дать побочный эффект — полиневрит. Для этой болезни характерно снижение мышечного тонуса, что вызывает онемение пальцев на ногах и руках. Если такое наблюдается, то препарат заменяют на Винбластин.
Также смена или отмена препаратов производится при возникновении осложнений в виде высокой температуры, диареи, рвоты.
Когда нужна пересадка
В некоторых случаях в период лечения необходима трансплантация костного мозга. Стволовые клетки пересаживают, когда здоровых организму недостаточно. Это может произойти при химиотерапии, так как препараты убивают не только злокачественные клетки, но и здоровые.
Для того чтобы пациент полностью исцелился, необходимо убрать все лейкемические клетки. После этого организм сможет вырабатывать нормальные.
Прогноз для жизни и рецидив болезни
Легче всего выздоровление наступает у пациентов от 2 до 10 лет. У людей в пожилом возрасте и у малышей до 1 года болезнь имеет высокий процент летального исхода.
.jpg)
За основу прогноза берется способность организма жить после лечения. На нее может оказывать влияние ряд факторов, например, возраст пациента, длительность патологии, тип болезни, степень поражения иных органов, уровень лейкоцитов в крови.
Сказать, сколько живут после терапии, довольно сложно. Пациент считается здоровым, если в течение 6 лет после окончания лечения у него не возникает рецидива недуга. Тогда прогноз на будущее благоприятный.
Для грудничков часто болезнь становится непреодолимой. Детский лимфобластный лейкоз имеет шансы пятилетней выживаемости около 90%. При этом наиболее благоприятный для исцеления возраст составляет 2-6 лет. Пациент из этой категории имеет в полтора раза больше шансов, чем остальные. Пятилетняя выживаемость у пожилых людей не более 55%.
Если возникает рецидив болезни, то прогноз ухудшается. Недуг может окончиться смертельным исходом или новым периодом ремиссии. Сложность ситуации объясняется тем, что в процесс вовлекается центральная нервная система.
Разновидности патологии
Различают хронический и острый лейкоз. Первый не переходит во второй. Острая форма редко совмещается с хронической. Для нее характерна трансплантация незрелых клеток, их стремительное размножение и рост. При этом процесс не поддается контролю, поэтому высока вероятность смертельного исхода.
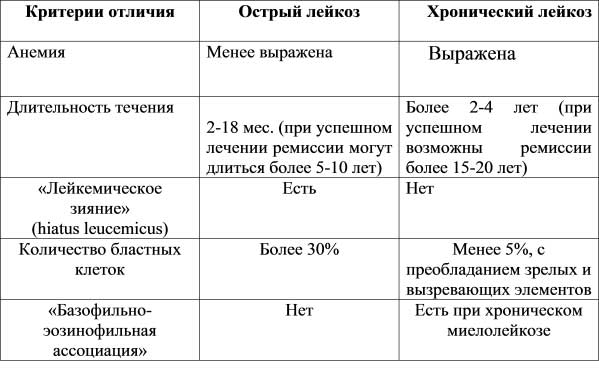
Хроническое течение характеризуется ростом видоизмененных готовых клеток или тех, которые находятся в стадии созревания. Длительность этой фазы значительно больше, чем острой формы. При хроническом течении недуга пациенту хватает поддерживающей терапии для восстановления здоровья.
Острая форма заболевания возникает в 75-85 случаях из 100. Врождённый рак может наблюдаться при мутации гена, сюда входят и болезни крови, синдром Дауна, генетическая наследственность. Удивительным фактом является то, что больше подвержены болезни те дети, которые выше и крупнее своих сверстников.
Острый лимфобластный лейкоз может быть как врожденным, так и приобретенным. Обычно если ребенок появляется на свет уже с этой патологией, то у него довольно низкий уровень выживаемости.
По характеру течения острый лейкоз делится на Т-клеточный и В-линейный. Это зависит от клеток, которые были предшественниками новообразования.
Лейкоциты, в свою очередь, классифицируются на гранулоцитарные и агранулоцитарные, зернистые и незернистые. Они подразделяются на эозинофилы, нейтрофилы, базофилы, лимфоциты, моноциты.
Основными рекомендациями врачей являются правильный состав питания, ведение активного образа жизни, отказ от вредных привычек, своевременное лечение всех возникающих патологий, особенно тех, которые способствуют развитию рака.
Суть болезни
Лейкоз, или лейкемия – заболевание костного мозга, в обиходе иногда называемое «раком крови». При лейкозе нарушено нормальное кроветворение: производится избыточное количество аномальных незрелых клеток крови, обычно предшественников лейкоцитов. Эти бластные клетки, размножаясь и накапливаясь в костном мозге, мешают выработке и функционированию нормальных клеток крови, что и обусловливает основные симптомы заболевания. Кроме того, эти опухолевые клетки могут накапливаться в лимфоузлах, печени, селезенке, центральной нервной системе и других органах, также вызывая появление специфических симптомов.
Как известно, различные клетки крови развиваются по-разному и имеют разных предшественников – то есть относятся к различным линиям кроветворения (см. схему в статье «Кроветворение»). Линия кроветворения, приводящая к появлению лимфоцитов, называется лимфоидной; остальные же лейкоциты относятся к миелоидной линии. Соответственно, различают лейкозы из клеток-предшественников лимфоцитов (такие лейкозы называют лимфобластными, лимфоцитарными или просто лимфолейкозами) и из предшественников других лейкоцитов (миелобластные, миелоидные, миелолейкозы).
Острый лимфобластный лейкоз (ОЛЛ) – самый распространенный вид лейкоза у детей, но это заболевание нередко встречается и во взрослом возрасте. Термин «острый» означает быстрое развитие болезни, в противоположность хроническому лейкозу. Термин «лимфобластный» означает, что незрелые клетки, составляющие основу болезни, являются лимфобластами, то есть предшественниками лимфоцитов.
Частота встречаемости и факторы риска
На долю ОЛЛ приходится 75-80% всех опухолевых заболеваний кроветворной системы у детей (3-4 случая на 100 тысяч детей в год). Именно ОЛЛ – самое распространенное онкологическое заболевание у детей. Чаще всего ОЛЛ возникает в возрасте до 14 лет; пик детской заболеваемости приходится на возраст 2-5 лет. У мальчиков эта болезнь встречается чаще, чем у девочек.
Вероятность возникновения ОЛЛ несколько повышена у людей, ранее получавших лечение от какой-либо другой болезни (обычно злокачественной опухоли) с использованием облучения или определенных видов цитостатической химиотерапии. Также риск ОЛЛ повышен у детей с некоторыми генетическими нарушениями – например, с синдромом Дауна, нейрофиброматозом типа I или первичными иммунодефицитными состояниями.
Риск заболеть для ребенка выше среднего, если у его брата- или сестры-близнеца уже был диагностирован лейкоз.
Впрочем, в большинстве случаев лейкоза не удается обнаружить никакого из перечисленных факторов риска, и причины, вызвавшие болезнь, остаются неизвестными.
Признаки и симптомы
ОЛЛ характеризуется множеством различных признаков и у разных больных может проявляться по-разному. Большинство наблюдаемых симптомов, однако, обусловлено тяжелыми нарушениями кроветворения: избыток аномальных бластных клеток при ОЛЛ сочетается с недостаточным количеством нормальных функциональных клеток крови.
Обычно наблюдаются слабость, бледность, снижение аппетита, потеря веса, учащенное сердцебиение (тахикардия) – проявления анемии и опухолевой интоксикации. Недостаток тромбоцитов проявляется мелкими кровоизлияниями на коже и слизистых оболочках, кровотечениями из десен, носовыми и кишечными кровотечениями, кровоподтеками, синяками. Из-за накопления бластных клеток часто увеличиваются лимфоузлы – в частности, шейные, подмышечные, паховые. Нередко увеличиваются также печень и селезенка — как говорят, возникает гепатоспленомегалия.
Часто наблюдаются боли в костях и суставах, иногда возникают патологические (то есть вызванные заболеванием) переломы костей. Из-за недостаточного количества нормальных зрелых лейкоцитов возможны частые инфекции. Повышение температуры может наблюдаться как в связи с возникшей на фоне лейкоза инфекцией, так и из-за опухолевой интоксикации. Иногда одним из проявлений острого лейкоза является продолжительная ангина, плохо поддающаяся терапии антибиотиками.
В некоторых случаях ОЛЛ вызывает изменения и в других органах: глазах, почках, яичках у мальчиков и яичниках у девочек, причем у мальчиков поражение половых органов наблюдается чаще. Нередко возникает поражение центральной нервной системы — нейролейкемия.
Так как все наблюдаемые симптомы могут быть связаны и с другими заболеваниями и не специфичны для ОЛЛ, перед началом лечения необходима лабораторная диагностика, которая в срочном порядке производится в больничных условиях.
Диагностика
При ОЛЛ возникают изменения в обычном клиническом анализе крови: понижены уровни эритроцитов и тромбоцитов, появляются бластные клетки. Очень высокий лейкоцитоз возможен, но, вопреки распространенному мнению, наблюдается не во всех случаях. В целом же надежно поставить диагноз можно только при исследовании образца костного мозга; для этой цели необходима костномозговая пункция.
При морфологическом исследовании диагноз «острый лимфобластный лейкоз» ставится при обнаружении более 25% бластных клеток в костном мозге. Но обязательно производятся более тонкие исследования: цитохимическое (окрашивание клеток, позволяющее более точно установить их природу), цитогенетическое (изучение строения хромосом в лейкемических клетках), иммунофенотипирование (изучение белковых молекул на поверхности клеток). Дело в том, что при диагностике очень важно не только надежно отличить ОЛЛ от острого миелоидного лейкоза, но и определить конкретный вариант ОЛЛ, поскольку он сильно влияет на терапию и прогноз заболевания.
Так, ОЛЛ может быть B-клеточным (около 80% случаев) и T-клеточным, в зависимости от того, относятся ли лейкемические клетки к B- или T-лимфоцитарной линии. В зависимости от «степени зрелости» бластных клеток среди как В-, так и Т-клеточных лейкозов выделяют несколько вариантов; их установление в ходе иммунофенотипирования важно для определения стратегии лечения.
В ходе диагностики ОЛЛ также необходимо исследовать состояние центральной нервной системы. Анализ спинномозговой жидкости (ликвора) позволяет определить, нет ли у больного поражения центральной нервной системы – нейролейкемии. Образец ликвора для анализа получают посредством пункции спинномозгового канала.
Возможны и дополнительные диагностические процедуры для исследования пораженных лимфоузлов и внутренних органов – компьютерная томография (КТ), ультразвуковое исследование (УЗИ) и так далее.
Диагностические исследования позволяют для каждого конкретного больного определить ту или иную группу риска, от которой зависят прогноз заболевания и планируемое лечение. Так, говорят о стандартном риске, высоком риске и т.д. Отнесение к той или иной группе зависит от многих факторов. Перечислим некоторые из них.
- Возраст больного: менее благоприятным считается возраст до 1 года или старше 10 лет.
- Количество лейкоцитов: риск увеличивается при очень высоком лейкоцитозе в момент диагноза.
- Т-клеточный ОЛЛ у детей обычно определяет более высокий риск (худший прогноз) по сравнению с В-клеточным.
- Хромосомные аномалии в лейкемических клетках, связанные с числом хромосом и транслокациями. При некоторых из них усложняется лечение болезни и ухудшается прогноз. Так, особенно неблагоприятна филадельфийская хромосома – транслокация t(9;22). В то же время, например, транслокация t(12;21) связана с относительно хорошим прогнозом.
- Распространение ОЛЛ в другие органы, помимо костного мозга (например, возникновение нейролейкемии), определяет более высокий риск.
- При раннем или повторном рецидиве лейкоза риск значительно повышается.
Лечение
Как упомянуто в предыдущем разделе, современное лечение ОЛЛ основано на разделении пациентов на группы риска – в зависимости от того, насколько вероятно у них достижение и сохранение ремиссии при одинаковой терапии. Соответственно, пациенты, относящиеся к группам более высокого риска (то есть те, у кого изначальный прогноз хуже), получают более интенсивную терапию, а в группах более низкого риска можно использовать менее интенсивную терапию и тем самым избегать излишней токсичности и тяжелых осложнений.
Терапия ОЛЛ, как правило, состоит из трех этапов:
Индукция ремиссии (то есть терапия, направленная на достижение ремиссии) проводится в течение нескольких первых недель лечения. Под ремиссией здесь подразумеваеся содержание менее 5% бластных клеток в костном мозге и отсутствие их в обычной (периферической) крови в сочетании с признаками восстановления нормального кроветворения.
В ходе индукции проводится интенсивная многокомпонентная химиотерапия лекарствами-цитостатиками, которые вызывают разрушение лейкемических клеток. На этом этапе могут применяться такие лекарства, как винкристин, гормоны-глюкокортикостероиды, аспарагиназа, антрациклины (даунорубицин и др.), иногда и другие препараты. Индукция позволяет достигнуть ремиссии более чем у 95% детей и у 75-90% взрослых с ОЛЛ.
Консолидация (закрепление) ремиссии направлена на уничтожение остаточных аномальных бластных клеток во избежание рецидива заболевания. Общая продолжительность этого этапа составляет несколько месяцев и сильно зависит от конкретного протокола лечения. В ходе курсов терапии на этапе консолидации могут использоваться метотрексат, 6-меркаптопурин, винкристин, преднизолон, а также циклофосфамид, цитарабин, даунорубицин, аспарагиназа и т.д.
На этапах индукции и консолидации введение химиотерапевтических препаратов производится в основном внутривенно, в условиях больничного стационара или стационара одного дня.
Поддерживающая терапия проводится для поддержания ремиссии, то есть для дополнительного снижения риска рецидива после этапов индукции и консолидации. Продолжительность поддерживающей терапии – 2-3 года. На этом этапе основными препаратами являются 6-меркаптопурин и метотрексат.
Поддерживающая терапия представляет собой этап наименее интенсивного лечения. Лекарства принимаются в виде таблеток, пребывание в больнице при этом не требуется.
Для лечения и профилактики нейролейкемии на перечисленных этапах химиопрепараты должны вводиться интратекально, то есть в спинномозговой канал посредством люмбальных пункций. Иногда лекарства вводят в желудочки (особые полости) головного мозга через специальный резервуар Оммайя, который устанавливается под кожей головы. Основной препарат, используемый для интратекального введения при ОЛЛ, — метотрексат; дополнительно также применяются цитарабин и глюкокортикостероиды. У некоторых пациентов используется и облучение головы – краниальное облучение.
Существует также понятие реиндукции: это периодически повторяемые уже после достижения ремиссии циклы полихимиотерапии, аналогичные используемым при индукции. Реиндукция позволяет дополнительно снизить число лейкемических клеток и тем самым повысить «надежность» ремиссии.
К сожалению, несмотря на все перечисленные меры, иногда возникает рецидив ОЛЛ – костномозговой, экстрамедуллярный (то есть вне костного мозга – например, с поражением центральной нервной системы или яичек) или комбинированный. В этом случае проводится противорецидивная терапия. Выбор протокола лечения рецидива зависит от сроков его возникновения (ранний или поздний) и от того, является ли рецидив костномозговым или экстрамедуллярным. К сожалению, при раннем рецидиве шансы на успех терапии значительно снижаются.
В ходе лечения ОЛЛ может применяться трансплантация костного мозга от родственного или неродственного донора. Если по плану лечения предусмотрена трансплантация, то ее проводят после достижения ремиссии. Как правило, трансплантация показана только при высоком риске (например, после раннего рецидива), поскольку вероятность хорошего ответа на стандартную терапию при ОЛЛ в среднем высока, особенно у детей.
Химиотерапия ОЛЛ высокоэффективна, но зачастую тяжело переносится и может быть связана с серьезными побочными эффектами. Так, в процессе лечения подавляется кроветворение и бывают необходимы переливания компонентов донорской крови – тромбоцитов во избежание кровотечений при очень низком уровне собственных тромбоцитов больного, эритроцитов для борьбы с анемией. Переливания донорских лейкоцитов (гранулоцитов) применяются только в редких случаях при тяжелых инфекционных осложнениях.
В числе «обычных» побочных эффектов химиотерапии можно также назвать тошноту, рвоту, облысение. Серьезнае проблема связана с возможностью аллергических реакций на химиопрепараты, вплоть до анафилактического шока – жизнеугрожающего состояния, которое характеризуется отеком, затруднением дыхания, сильным зудом и т.д. Так, сравнительно часто встречается аллергия на аспарагиназу, и может быть необходимо использование аналогов этого препарата (онкаспар, эрвиназа).
Поскольку и лейкоз сам по себе, и используемая при его лечении химиотерапия резко снижают сопротивляемость организма различным инфекциям, то больным во время лечения необходимы эффективные антибактериальные и противогрибковые лекарства для профилактики и терапии инфекционных осложнений. Опасны как обычные, так и оппортунистические инфекции. В частности, серьезную проблему представляют такие грибковые инфекции, как кандидоз и аспергиллез.
Интенсивное лечение ОЛЛ накладывает серьезные ограничения на образ жизни больного. Необходимо соблюдать определенную диету и строгие гигиенические требования. Во избежание инфекций ограничиваются контакты с внешним миром. При очень низком уровне тромбоцитов нельзя не только допускать травмы, но даже, например, чистить зубы зубной щеткой — чтобы не спровоцировать кровотечение из десен. После достижения ремиссии строгость этих ограничений постепенно снижается. Врачи и медсестры сообщают каждому больному, что ему можно и что нельзя на текущем этапе лечения.
Прогноз
Без лечения ОЛЛ приводит к гибели больного в течение нескольких месяцев или даже недель. Однако использование современных протоколов лечения дает при ОЛЛ очень хороший результат: можно вылечить около 80% больных детей (некоторые источники приводят и более высокие цифры — например, до 85%). У взрослых, особенно пожилых, результаты хуже, но, тем не менее, примерно у 40% взрослых больных удается достичь стойкой ремиссии – то есть отсутствия рецидивов болезни в течение пяти и более лет, после чего человека можно считать здоровым.