Содержание:
282-283


Ткани и органы. Кровь
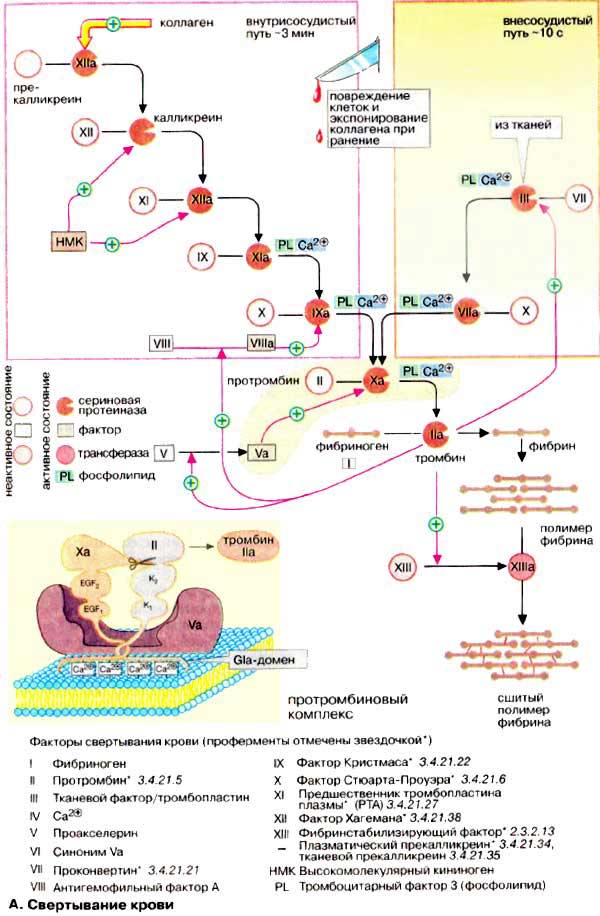 При нарушении целостности кровеносной системы уменьшение кровопотери обеспечивает система гемостаза. Гемостаз поддерживается двумя путями: остановкой кровотечения с помощью тромбоцитов и свертыванием крови . В данном разделе основное внимание уделено ферментативным реакциям свертывания крови. Повторное растворение сгустков крови, фибринолиз , рассмотрен на с. 284.
При нарушении целостности кровеносной системы уменьшение кровопотери обеспечивает система гемостаза. Гемостаз поддерживается двумя путями: остановкой кровотечения с помощью тромбоцитов и свертыванием крови . В данном разделе основное внимание уделено ферментативным реакциям свертывания крови. Повторное растворение сгустков крови, фибринолиз , рассмотрен на с. 284.
Номенклатура факторов свертывания крови несколько запутана. Факторы нумеруются римскими цифрами, при этом активированная форма фактора в наименовании содержит дополнительно букву «а» после римской цифры. Многие факторы являются протеиназами. На схеме неактивные предшественники протеиназ представлены в виде окружностей, а активные ферменты — окрашенными кружочками с вырезанным сектором. Вспомогательные факторы показаны в виде прямоугольников.
При свертывании крови происходит ферментативное превращение растворимого белка плазмы фибриногена (фактора I, см. рис. 71) в фибриновый полимер, сеть волокон нерастворимого белка. В этой реакции принимает участие фермент тромбин (фактор IIа), который протеолитически отщепляет от молекулы фибриногена небольшой пептидный фрагмент, в результате чего освобождаются участки связывания, что позволяет молекуле фибрина агрегировать в полимер . Затем с помощью глутамин-трансферазы (фактора XIII) образуются изопептидные связи боковых цепей аминокислот фибрина, что приводит к формированию нерастворимого фибринового сгустка (тромба).
Свертывание крови может запускаться двумя различными путями: вследствие нарушения целостности ткани ( внесосудистый путь, на схеме справа) или процессами, которые начинаются на внутренней поверхности сосуда ( внутрисосудистый путь , на схеме слева). В обоих случаях запускается каскад протеолитических реакций: из неактивных предшественников ферментов (зимогенов, условно обозначаемых на схеме окружностями) путем отщепления пептидов образуются активные сериновые протеиназы (обозначаемые на схеме окрашенными кружочками с вырезанным сектором), которые в свою очередь действуют на другие белки. Оба реакционных пути нуждаются в ионах Са 2+ и фосфолипидах [ФЛ (PL)] и оба завершаются активацией фактором Ха протромбина (фактора II) с образованием тромбина (IIа).
Внутрисосудистый путь инициируется коллагеном, который в норме не экспонирован на внутренней поверхности кровеносных сосудов; его контакт с кровью приводит к активации фактора XII. Внесосудистый путь активации начинается с освобождения фактора III (тканевого тромбопластина) из поврежденных клеток ткани. В течение нескольких секунд этот фактор приводит к свертыванию крови в области раны.
Факторы свертывания II, VII, IX и X содержат необычную аминокислоту, γ-карбоксиглутаминовую (Gla). Остатки Gla, которые образуются в результате посттрансляционного карбоксилирования остатков глутаминовой кислоты, группируются в особых белковых доменах. Они присоединяют ионы Са 2+ и вследствие этого связывают соответствующие регуляторные факторы с фосфолипидами на поверхности плазматической мембраны. На рисунке это схематически представлено на примере протромбинового комплекса (Va, Ха и II). Вещества, способные связывать свободные ионы Са 2+ в виде комплекса, например цитрат, предотвращают это взаимодействие с фосфолипидами и тормозят свертывание. Для синтеза остатков Gla необходим в качестве кофактора витамин К (см. с. 342). Антагонисты витамина К, такие, как дикумарин, подавляют синтез активных факторов коагуляции и действуют поэтому также как ингибиторы свертывания.
Генетически обусловленный дефицит отдельных факторов свертывания приводит к кровоточивости (гемофилия).
Контроль за свертыванием крови (не показан на схеме). Процесс свертывания крови находится в постоянном равновесии между активацией и торможением. Для торможения в плазме имеются очень эффективные ингибиторы протеиназ. Сериновые протеиназы системы свертывания инактивируются антитромбином. Его действие усиливается сульфатированным глюкозаминогликаном — гепарином (см. с. 336). Тромбомодулин, расположенный на внутренней стенке кровеносных сосудов, инактивирует тромбин, образуя с ним стехиометрический комплекс. За протеолитическое разрушение факторов V и VIII в плазме отвечает белок с. Этот белок в свою очередь активируется тромбином и, тем самым, реализуется самотормозящийся механизм свертывания крови.
Важнейшим этапом остановки кровотечения (гемостаза) является свертывание крови. Это очень сложный ферментативный процесс, в результате которого белок крови фибриноген превращается в фибрин, образуя сгусток. Среднее время образования такого сгустка у здорового человека — около 10 минут.
Как происходит свертывание?
Кровь, выпущенная из кровеносного сосуда, начинает свертываться уже за три-четыре минуты. Еще через две минуты образуется твердый сгусток студенистой консистенции. Значит в этом процессе важен именно временной промежуток: если сгусток образуется позже, организм потеряет много крови. Таким образом, свертывание крови — это важнейший физиологический процесс, препятствующий кровопотере.
Уменьшение способности крови к свертыванию опасно для человека: даже незначительная травма может обернуться для него большой, порой невосполнимой кровопотерей. И, наоборот, повышенная кровосвертывающая способность организма приводит к тому, что внутри сосудов начинают образовываться сгустки — тромбы. Они приводят к закупорке сосудов.
Нормальный процесс свертывания крови, таким образом, обеспечивает постоянство ее объема в кровяном русле.
Механизм свертывания происходит с помощью изменения физических и химических характеристик крови, основанного на превращении белка фибриногена в фибрин. Фибрин выпадает в виде тонких нитей, способных образовывать сеть. Такая сеть задерживает форменные элементы крови. Тромбоциты еще больше уплотняют кровяной сгусток.
В 1861 г. А. А. Шмидт установил, что превращение растворенного в плазме фибриногена в нерастворимый фибрин проходит под воздействием тромбина, особого фермента. В крови постоянно содержится протромбин, образующийся в печени. Он начинает превращаться в тромбин под воздействием тромбопластина, образующегося во время разрушения тромбоцитов и при повреждении других клеток. В этом процессе также участвуют факторы свертывания крови, в том числе вещества, высвобождающиеся из тромбоцитов. Теория А. А. Шмидта выделяет три стадии этого сложного процесса.
- На первой стадии формируется протромбиназа, активирующая белок протромбин. Происходит образование тканевого тромбопластина в ответ на повреждение стенок сосуда. Во время разрушения кровяных пластинок образуется кровяная протромбиназа. Это очень сложный процесс, в котором задействованы тромбоцитарные и плазменные факторы.
- На второй стадии протромбин переходит в активный тромбин.
- На завершающей стадии происходит превращение фибриногена в фибрин. На его нитях и оседают элементы крови, закрывающие рану.
Процесс свертывания крови невозможен без формирования такого сгустка. При этом запускается свыше 30 различных химических и физиологических реакций. Всего же выделяют три типа кровяных сгустков:
- белый тромб, состоящий из тромбоцитов и фибрина и появляющийся главным образом в артериях;
- диссеминированные отложения фибрина, образующиеся в капиллярах;
- красные тромбы появляются в сосудах с неизмененными стенками при замедленном кровотоке.

Факторы свертывания
В крови содержатся вещества, без которых невозможен гемостаз, то есть остановка кровотечения. Это факторы свертывания крови. Большинство из них — это белки. Кроме того, к ним причисляют низкомолекулярные вещества, а также ионы кальция.
Существует 35 факторов свертывания, из них — 13 плазменных и 22 тромбоцитарных. Плазменные факторы обозначаются римскими цифрами, а тромбоцитарные — арабскими.
Плазменные факторы имеют белковую природу. Белковые факторы в норме неактивны. Их активация происходит за счет сложных химических реакций. Все плазменные факторы свертывания крови делятся на две группы: зависимые от витамина К (образуются в печени под воздействием этого витамина) и независимые от витамина К (для их синтеза это вещество не требуется).
Многие факторы, способствующие свертыванию, обнаруживаются в эритроцитах, а также в лейкоцитах. Во время этого процесса физиологическая роль эритроцитов огромна: они содержат вещества, способствующие быстрому образованию кровяного сгустка. То же относится и к лейкоцитам.
В тканях также содержатся необходимые вещества, от которых зависит свертывание крови. В первую очередь, это тромбопластин. Он в большом количестве содержится в легких, коре головного мозга, плаценте, сосудистом эндотелии.
Важнейшие тромбоцитарные факторы выполняют в организме такую роль:
- ускоряют образование тромбина;
- ускоряют превращение фибриногена в нерастворимый фибрин;
- устраняют действие антикоагулянтов;
- способствуют сокращению кровяного сгустка;
- оказывают сосудосуживающее действие;
- способствуют агрегации тромбоцитов (то есть процессу их «склеивания», необходимому для быстрой остановки кровотечения).
Комплексное действие этих веществ способствует ускорению свертывания.
Причины несвертываемости крови, и можно ли от этого избавиться?
Подробнее о пользе железа в крови читайте в этой статье.
Нарушения свертывания
При этих болезнях свертывание крови бывает слишком медленным или, наоборот, слишком быстрым. Способствуют свертыванию такие факторы:
- болевые раздражения;
- действие адреналина, ускоряющего этот процесс и сужающего кровеносные сосуды;
- достаточное количество витамина К и кальция в крови.
- наличие в клетках печени и легких гепарина, препятствующего образованию тромбопластина;
- наличие в сыворотке фибринолизина, растворяющего фибрин;
- низкая температура;
- наличие в крови солей щавелевой и лимонной кислот;
- использование медицинских пиявок.
Замедление свертывания (например, при гемофилии, болезни Верльгофа и др.) приводит к патологическим кровотечениям. Наиболее характерные симптомы таких болезней:
- проблемы с остановкой любого кровотечения;
- появление на теле синяков разного размера;
- возникновение гематом даже после незначительной травмы;
- частые носовые кровотечения;
- кровоточивость десен.
При гемофилии свертывание крови существенно изменяется. При этом в организме нарушается образование тромбопластина. Это заболевание наследуется по сцепленному с полом рецессивному типу. Болеют только лица мужского пола. Женщины же являются носителями данной болезни, и у них она не проявляется, но передается через них по наследству. В крови обнаруживается недостаток VIII, IX и XI факторов.
Эта болезнь проявляется в раннем возрасте. Обнаруживаются кровотечения из носа и десен, суставные кровоизлияния. Больным необходимы эффективные терапевтические меры, так как даже небольшие кровотечения чреваты серьезными последствиями. Им чаще всего вводят антигемофильную плазму, антигемофильный глобулин, производят переливание крови.
При тромбоцитопении количество тромбоцитов уменьшается, а свертывание крови замедляется. У больных наблюдаются кровоточивость и проблемы с остановкой кровотечения. Характерно частое возникновение носовых кровотечений, а также выделение крови из микротравм слизистой оболочки рта. Больные с острой формой тромбоцитопении подлежат госпитализации.
Тромбоцитопеническая пурпура (болезнь Верльгофа) относится к аутоиммунным болезням. Характерны:
- кожные геморрагии;
- кровоизлияния в слизистые оболочки;
- гематурия;
- «дегтеобразный» стул.
При ускорении свертываемости у человека возникает повышенный риск образования тромбов. Внутри кровеносных сосудов образуются сгустки. Они препятствуют нормальному прохождению крови. Возможно свободное перемещение кровяных сгустков по сосудам.
Опаснейшее осложнение тромбоза — эмболия. Происходит закупорка сосудов, вызывающая кислородное голодание и смерть клеток. Особое место среди таких патологий занимает тромбоэмболия легочной артерии. Болезнь характеризуется яркой выраженностью симптомов. В случае неоказания больному врачебной помощи возможна смерть.
Итак, свертывание крови — важнейший физиологический процесс, обеспечивающий нормальную жизнедеятельность организма.
Свёртывание крови — это важнейший этап работы системы гемостаза, отвечающий за остановку кровотечения при повреждении сосудистой системы организма. Совокупность взаимодействующих между собой весьма сложным образом различных факторов свёртывания крови образует систему свёртывания крови.
Свёртыванию крови предшествует стадия первичного сосудисто-тромбоцитарного гемостаза. Этот первичный гемостаз почти целиком обусловлен сужением сосудов и механической закупоркой агрегатами тромбоцитов места повреждения сосудистой стенки. Характерное время для первичного гемостаза у здорового человека составляет 1—3 минуты. Собственно свёртыванием крови (гемокоагуляция, коагуляция, плазменный гемостаз, вторичный гемостаз) называют сложный биологический процесс образования в крови нитей белка фибрина, который полимеризуется и образует тромбы, в результате чего кровь теряет текучесть, приобретая творожистую консистенцию. Свёртывание крови у здорового человека происходит локально, в месте образования первичной тромбоцитарной пробки. Характерное время образования фибринового сгустка — около 10 минут . Свёртывание крови — ферментативный процесс.
Основоположником современной физиологической теории свёртывания крови является Александр Шмидт. В научных исследованиях XXI века , проведённых на базе Гематологического научного центра под руководством Атауллаханова Ф. И. , было убедительно показано [1] [2] , что свёртывание крови представляет собой типичный автоволновой процесс, в котором существенная роль принадлежит эффектам бифуркационной памяти.
Содержание
Физиология [ править | править код ]

Процесс гемостаза сводится к образованию тромбоцитарно-фибринового сгустка. Условно его разделяют на три стадии [3] :
- временный (первичный) спазм сосудов;
- образование тромбоцитарной пробки за счёт адгезии и агрегации тромбоцитов;
- ретракция (сокращение и уплотнение) тромбоцитарной пробки.
Повреждение сосудов сопровождается немедленной активацией тромбоцитов. Адгезия (прилипание) тромбоцитов к волокнам соединительной ткани по краям раны обусловлена гликопротеином фактором Виллебранда [4] . Одновременно с адгезией наступает агрегация тромбоцитов: активированные тромбоциты присоединяются к повреждённым тканям и друг к другу, формируя агрегаты, преграждающие путь потере крови. Появляется тромбоцитарная пробка [3] .
Из тромбоцитов, подвергшихся адгезии и агрегации, усиленно секретируются различные биологически активные вещества (АДФ, адреналин, норадреналин и другие), которые приводят к вторичной, необратимой агрегации. Одновременно с высвобождением тромбоцитарных факторов происходит образование тромбина [3] , который воздействует на фибриноген с образованием сети фибрина, в которой застревают отдельные эритроциты и лейкоциты – образуется так называемый тромбоцитарно-фибриновый сгусток (тромбоцитарная пробка). Благодаря контрактильному белку тромбостенину тромбоциты подтягиваются друг к другу, тромбоцитарная пробка сокращается и уплотняется, наступает её ретракция [3] .
Процесс свёртывания крови [ править | править код ]


Процесс свёртывания крови представляет собой преимущественно проферментно-ферментный каскад, в котором проферменты, переходя в активное состояние, приобретают способность активировать другие факторы свёртывания крови [3] . В самом простом виде процесс свёртывания крови может быть разделён на три фазы:
- фаза активации включает комплекс последовательных реакций, приводящих к образованию протромбиназы и переходу протромбина в тромбин;
- фаза коагуляции — образование фибрина из фибриногена;
- фаза ретракции — образование плотного фибринового сгустка.
Данная схема была описана ещё в 1905 году [5] Моравицем и до сих пор не утратила своей актуальности [6] .
В области детального понимания процесса свёртывания крови с 1905 года произошёл значительный прогресс. Открыты десятки новых белков и реакций, участвующих в процессе свёртывания крови, который имеет каскадный характер. Сложность этой системы обусловлена необходимостью регуляции данного процесса.
Современное представление с позиций физиологии каскада реакций, сопровождающих свёртывание крови, представлено на рис. 2 и 3. Вследствие разрушения тканевых клеток и активации тромбоцитов высвобождаются белки фосфолипопротеины, которые вместе с факторами плазмы Xa и Va, а также ионами Ca 2+ образуют ферментный комплекс, который активирует протромбин. Если процесс свёртывания начинается под действием фосфолипопротеинов, выделяемых из клеток повреждённых сосудов или соединительной ткани, речь идёт о внешней системе свёртывания крови (внешний путь активации свёртывания, или путь тканевого фактора). Основными компонентами этого пути являются 2 белка: фактор VIIа и тканевый фактор, комплекс этих 2 белков называют также комплексом внешней теназы.
Если же инициация происходит под влиянием факторов свёртывания, присутствующих в плазме, используют термин внутренняя система свёртывания. Комплекс факторов IXа и VIIIa, формирующийся на поверхности активированных тромбоцитов, называют внутренней теназой. Таким образом, фактор X может активироваться как комплексом VIIa—TF (внешняя теназа), так и комплексом IXa—VIIIa (внутренняя теназа). Внешняя и внутренняя системы свёртывания крови дополняют друг друга [5] .
В процессе адгезии форма тромбоцитов меняется — они становятся округлыми клетками с шиповидными отростками. Под влиянием АДФ (частично выделяется из повреждённых клеток) и адреналина способность тромбоцитов к агрегации повышается. При этом из них выделяются серотонин, катехоламины и ряд других веществ. Под их влиянием происходит сужение просвета повреждённых сосудов, возникает функциональная ишемия. В конечном итоге сосуды перекрываются массой тромбоцитов, прилипших к краям коллагеновых волокон по краям раны [5] .
На этой стадии гемостаза под действием тканевого тромбопластина образуется тромбин. Именно он инициирует необратимую агрегацию тромбоцитов. Реагируя со специфическими рецепторами в мембране тромбоцитов, тромбин вызывает фосфорилирование внутриклеточных белков и высвобождение ионов Ca 2+ .
При наличии в крови ионов кальция под действием тромбина происходит полимеризация растворимого фибриногена (см. фибрин) и образование бесструктурной сети волокон нерастворимого фибрина. Начиная с этого момента в этих нитях начинают фильтроваться форменные элементы крови, создавая дополнительную жёсткость всей системе, и через некоторое время образуя тромбоцитарно-фибриновый сгусток (физиологический тромб), который закупоривает место разрыва, с одной стороны, предотвращая потерю крови, а с другой — блокируя поступление в кровь внешних веществ и микроорганизмов. На свёртывание крови влияет множество условий. Например, катионы ускоряют процесс, а анионы — замедляют. Кроме того, существуют вещества как полностью блокирующие свёртывание крови (гепарин, гирудин и другие), так и активирующие его (яд гюрзы, феракрил).
Врождённые нарушения системы свёртывания крови называют гемофилией.
Методы диагностики свёртывания крови [ править | править код ]
Все многообразие клинических тестов свёртывающей системы крови можно разделить на две группы [7] :
- глобальные (интегральные, общие) тесты;
- «локальные» (специфические) тесты.
Глобальные тесты характеризуют результат работы всего каскада свёртывания. Они подходят для диагностики общего состояния свёртывающей системы крови и выраженности патологий, с одновременным учётом всех привходящих факторов влияний. Глобальные методы играют ключевую роль на первой стадии диагностики: они дают интегральную картину происходящих изменений в свёртывающей системе и позволяют предсказывать тенденцию к гипер- или гипокоагуляции в целом. «Локальные» тесты характеризуют результат работы отдельных звеньев каскада свёртывающей системы крови, а также отдельных факторов свёртывания. Они незаменимы для возможного уточнения локализации патологии с точностью до фактора свёртывания. Для получения полной картины работы гемостаза у пациента врач должен иметь возможность выбирать, какой тест ему необходим.
- определение времени свёртывания цельной крови (методы Сухарева, Мас-Магро, Моравица);
- тромбоэластография;
- тест генерации тромбина (тромбиновый потенциал, эндогенный тромбиновый потенциал);
- тромбодинамика.
- активированное частичное тромбопластиновое время (АЧТВ);
- тест протромбинового времени (или протромбиновый тест, МНО, ПВ);
- узкоспециализированные методы для выявления изменений в концентрации отдельных факторов.
Все методы, измеряющие промежуток времени с момента добавления реагента (активатора, запускающего процесс свёртывания) до формирования фибринового сгустка в исследуемой плазме, относятся к клоттинговым методам (от англ. сlot — сгусток).
Нарушения свёртывания крови [ править | править код ]
Нарушения свёртываемости крови могут быть обусловлены дефицитом одного или нескольких факторов свёртывания крови, появлением в циркулирующей крови их иммунных ингибиторов