Содержание:
В воде всегда присутствует немного катионов водорода и гидроксид-ионов, которые образуются в результате обратимой диссоциации:
H2O 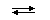 H + + OH —
H + + OH —
Водородный показатель рН характеризует концентрацию свободных ионов водорода в воде.
Величина рН определяется количественным соотношением в воде ионов Н + и ОН — , образующихся при диссоциации воды. Если в воде пониженное содержание свободных ионов водорода (рН>7) по сравнению с ионами ОН — , то вода будет иметь щелочную реакцию, а при повышенном содержании ионов Н + (рН 4,4 – желтый; лакмус при рН 8 – синий и т.д. Более точно (до сотых долей) значение рН можно определить с помощью специальных приборов – рН-метров. Такие приборы измеряют электрический потенциал специального электрода, погруженного в раствор; этот потенциал зависит от концентрации ионов водорода в растворе, и его можно измерить с высокой точностью.
Интересно сравнить значения рН растворов различных кислот, оснований, солей (при концентрации 0,1 моль/л), а также некоторых смесей и природных объектов.
| Некоторые значения pH | |
| Вещество | pH |
| Электролит в свинцовых аккумуляторах | 13 |
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Для студента самое главное не сдать экзамен, а вовремя вспомнить про него. 9745 —  | 7371 —
| 7371 —  или читать все.
или читать все.
91.146.8.87 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
Водоро́дный показа́тель, pH (лат. pondus Hydrogenii [1] — «вес водорода»; произносится «пэ-аш») — мера активности (в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, количественно выражающая его кислотность. Равен по модулю и противоположен по знаку десятичному логарифму активности водородных ионов, выраженной в молях на один литр:
pH = − lg [ H + ] <\displaystyle <\mbox
Содержание
История [ править | править код ]
Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель называется pH, по первым буквам латинских слов potentia hydrogeni — сила водорода, или pondus hydrogeni — вес водорода. Вообще в химии сочетанием pX принято обозначать величину, равную −lg X: Например, силу кислот часто выражают в виде pKa = −lg Ka.
В случае pH, буква H обозначает концентрацию ионов водорода (H + ), или, точнее, термодинамическую активность гидроксоний-ионов.
Уравнения, связывающие pH и pOH [ править | править код ]
Вывод значения pH [ править | править код ]
В чистой воде концентрации ионов водорода ([H + ]) и гидроксид-ионов ([OH − ]) одинаковы и при 22 °C составляют по 10 −7 моль/л, это напрямую следует из определения ионного произведения воды, которое равно [H + ] · [OH − ] и составляет 10 −14 моль²/л² (при 25 °C).
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается (на самом деле увеличивается не концентрация собственно ионов — иначе как способность кислот «присоединять» ион водорода могла бы приводить к этому — а концентрация именно таких соединений с «присоединённым» к кислоте ионом водорода), а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H + ] > [OH − ] говорят, что раствор является кислотным, а при [OH − ] > [H + ] — основным.
Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентраций ионов водорода пользуются их десятичным логарифмом, взятым с обратным знаком, который, собственно, и является водородным показателем — pH.
pH = − lg [ H + ] <\displaystyle <\mbox
pOH [ править | править код ]
Несколько меньшее распространение получила обратная pH величина — показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH − :
как в любом водном растворе при 25 °C [ H + ] [ OH − ] = 1 , 0 ⋅ 10 − 14 <\displaystyle [<\text
pOH = 14 − pH <\displaystyle <\text
Значения pH в растворах различной кислотности [ править | править код ]
| Вещество | pH | Цвет индикатора |
|---|---|---|
| Геотермальная вода у вулкана Даллол | ≈ 0 | |
| Электролит в свинцовых аккумуляторах | [2] | |
| Чистая вода при 25 °C | 7,0 | |
| Кровь | 7,36–7,44 | |
| Морская вода | 8,0 | |
| Мыло (жировое) для рук | 9,0–10,0 | |
| Нашатырный спирт | 11,5 | |
| Отбеливатель (хлорная известь) | 12,5 | |
| Концентрированные растворы щелочей | >13 |
Так как при 25 °C (стандартных условиях) [H + ] · [OH − ] = 10 −14 , то понятно, что при этой температуре pH + pOH = 14.
Так как в кислотных растворах [H + ] > 10 −7 , то у кислотных растворов pH 7, pH нейтральных растворов равен 7. При более высоких температурах константа электролитической диссоциации воды повышается, соответственно увеличивается ионное произведение воды, поэтому нейтральной оказывается pH + , так и OH − ); при понижении температуры, напротив, нейтральная pH возрастает.
Методы определения значения pH [ править | править код ]
Для определения значения pH растворов широко используют несколько методик. Водородный показатель можно приблизительно оценивать с помощью индикаторов, точно измерять pH-метром или определять аналитически путём, проведением кислотно-основного титрования.
- Для грубой оценки концентрации водородных ионов широко используются кислотно-основные индикаторы — органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах — либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1-2 единицы.
- Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислотной области в основную. Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.
- Использование специального прибора — pH-метра — позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью индикаторов. Ионометрический метод определения pH основывается на измерении милливольтметром-ионометром ЭДС гальванической цепи, включающей специальный стеклянный электрод, потенциал которого зависит от концентрации ионов H + в окружающем растворе. Способ отличается удобством и высокой точностью, особенно после калибровки индикаторного электрода в избранном диапазоне рН, позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
- Аналитический объёмный метод — кислотно-основное титрование — также даёт точные результаты определения кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакция. Точка эквивалентности — момент, когда титранта точно хватает, чтобы полностью завершить реакцию, — фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется кислотность раствора.
- Влияние температуры на значения pH
0,001 моль/Л HCl при 20 °C имеет pH=3, при 30 °C pH=3 [ источник не указан 1180 дней ]
0,001 моль/Л NaOH при 20 °C имеет pH=11,73, при 30 °C pH=10,83 [ источник не указан 1180 дней ]
Влияние температуры на значения pH объясняется различной диссоциацией ионов водорода (H + ) и не является ошибкой эксперимента. Температурный эффект невозможно компенсировать за счет электроники pH-метра.
Роль pH в химии и биологии [ править | править код ]
Кислотность среды имеет важное значение для множества химических процессов, и возможность протекания или результат той или иной реакции часто зависит от pH среды. Для поддержания определённого значения pH в реакционной системе при проведении лабораторных исследований или на производстве применяют буферные растворы, которые позволяют сохранять практически постоянное значение pH при разбавлении или при добавлении в раствор небольших количеств кислоты или щёлочи.
Водородный показатель pH широко используется для характеристики кислотно-основных свойств различных биологических сред.
Кислотность реакционной среды особое значение имеет для биохимических реакций, протекающих в живых системах. Концентрация в растворе ионов водорода часто оказывает влияние на физико-химические свойства и биологическую активность белков и нуклеиновых кислот, поэтому для нормального функционирования организма поддержание кислотно-основного гомеостаза является задачей исключительной важности. Динамическое поддержание оптимального pH биологических жидкостей достигается благодаря действию буферных систем организма.
В человеческом организме в различных органах водородный показатель различен.
Водоро́дный показа́тель, pH (произносится «пэ аш», от аббревиатуры англ. pH — произносится piː’eɪtʃ «Пи эйч») — мера активности ионов водорода в растворе, и количественно выражающая его кислотность. В очень разбавленных растворах активность ионов эквивалентна их концентрации).
pH вычисляют как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов, выраженной в молях на литр: $$\mbox
- «Кислые» значения рН и Кислый вкус в обыденном понимании ассоциируется с понятием Кислота. Однако с точки зрения современной науки (химии и биохимии) эти взаимосвязанные понятия существенно различны; существуют нерастворимые (и «не кислые») кислоты, и даже кислоты без ионов ([H + ]).
Содержание
История [ править ]
Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель называется pH, по первым буквам латинских слов potentia hydrogeni — сила водорода, или pondus hydrogenii — вес водорода. Вообще в химии сочетанием pX принято обозначать величину, равную -lgX, а буква H в данном случае обозначает концентрацию ионов водорода (H + ), или, точнее, термодинамическую активность оксоний-ионов.
Уравнения, связывающие pH и pOH [ править ]
Вывод значения pH [ править ]
В чистой воде при 25 °C концентрации ионов водорода ([H + ]) и гидроксид-ионов ([OH − ]) одинаковы и составляют 10 −7 моль/л, это напрямую следует из определения ионного произведения воды, которое равно [H + ] · [OH − ] и составляет 10 −14 моль²/л² (при 25 °C).
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H + ] > [OH − ] говорят, что раствор является кислым, а при [OH − ] > [H + ] — щелочным.
Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентраций ионов водорода пользуются их десятичным логарифмом, взятым с обратным знаком, который собственно и является водородным показателем — pH. $$\mbox
pOH [ править ]
Несколько меньшее распространение получила обратная pH величина — показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH − : $$\mbox
Значения pH в растворах различной кислотности [ править ]
- Вопреки распространённому мнению, pH может изменяться не только в интервале от 0 до 14, а может и выходить за эти пределы. Например, при концентрации ионов водорода [H + ] = 10 −15 моль /л, pH = 15, при концентрации ионов гидроксида 10 моль /л pOH = −1.
| Вещество | pH |
|---|---|
| Электролит в свинцовых аккумуляторах | 13 |
Так как при 25 °C (стандартных условиях)[H + ] · [OH − ] = 10 −14 , то понятно, что при этой температуре pH + pOH = 14.
Так как в кислых растворах [H + ] > 10 −7 , то pH кислых растворов pH 7, pH нейтральных растворов равен 7. При более высоких температурах константа электролитической диссоциации воды повышается, соответственно увеличивается ионное произведение воды, поэтому нейтральной оказывается pH + , так и OH − ); при понижении температуры, напротив, нейтральная pH возрастает.
Методы определения значения pH [ править ]
Для определения значения pH растворов широко используют несколько методик. Водородный показатель можно приблизительно оценивать с помощью индикаторов, точно измерять pH-метром или определять аналитически путём, проведением кислотно-основного титрования.
- Для грубой оценки концентрации водородных ионов широко используются кислотно-основные индикаторы — органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах — либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1—2 единицы.
Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислой области в щелочную. Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.
- Использование специального прибора — pH-метра — позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью индикаторов. Ионометрический метод определения pH основывается на измерении милливольтметром-ионометром ЭДС гальванической цепи, включающей специальный стеклянный электрод, потенциал которого зависит от концентрации ионов H + в окружающем растворе. Способ отличается удобством и высокой точностью, особенно после калибровки индикаторного электрода в избранном диапазоне рН, позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
- Аналитический объёмный метод — кислотно-основное титрование — также даёт точные результаты определения кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакции. Точка эквивалентности — момент, когда титранта точно хватает, чтобы полностью завершить реакцию, — фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется кислотность раствора.
- Влияние температуры на значения pH
0.001 моль/Л HCl при 20 °C имеет pH=3, при 30 °C pH=3
0.001 моль/Л NaOH при 20 °C имеет pH=11.73, при 30 °C pH=10.83
Влияние температуры на значения pH объяснятеся различной диссоциацией ионов водорода (H + ) и не является ошибкой эксперимента. Температурный эффект невозможно компенсировать за счет электроники pH-метра. [?]
Роль pH в химии и биологии [ править ]
Кислотность среды имеет важное значение для множества химических процессов, и возможность протекания или результат той или иной реакции часто зависит от pH среды. Для поддержания определённого значения pH в реакционной системе при проведении лабораторных исследований или на производстве применяют буферные растворы, которые позволяют сохранять практически постоянное значение pH при разбавлении или при добавлении в раствор небольших количеств кислоты или щёлочи.
Водородный показатель pH широко используется для характеристики кислотно-основных свойств различных биологических сред.
Кислотность реакционной среды особое значение имеет для биохимических реакций, протекающих в живых системах. Концентрация в растворе ионов водорода часто оказывает влияние на физико-химические свойства и биологическую активность белков и нуклеиновых кислот, поэтому для нормального функционирования организма поддержание кислотно-основного гомеостаза является задачей исключительной важности. Динамическое поддержание оптимального pH биологических жидкостей достигается благодаря действию буферных систем организма.
См. также [ править ]
Литература [ править ]
- Бейтс Р., Определение рН. Теория и практика, пер. 2 изд., Перевод с английского под редакцией акад. Б. П. Никольского и проф. М. М. Шульца. «Химия». Л., 1972
Комментарии [ править ]
Об источнике [ править ]
В 1965 г. Роджер Бейтс пишет проф. Б. П. Никольскому и проф. М. М. Шульцу:
Глубокоуважаемые профессора Никольский и Шульц! Занимаясь стандартизацией измерений pH, я смог по достоинству оценить ваши превосходные работы по стеклянному электроду, которые значительно расширили понимание механизма действия иона водорода. Я надеюсь в скором времени получить возможность побывать в вашей стране в связи с Московским конгрессом Международного союза общей и прикладной химии. Я был бы очень признателен вам, если бы смог посетить ваш институт и познакомиться с вами. Предполагая, что сессия конгресса закончится 18 июля, я надеюсь быть в Ленинграде 19 июля. Возможно ли моё посещение Вашего института 20 или 21 июля? Я хорошо знаком также с некоторыми работами доктора Л. Л. Макарова и, если это удобно, хотел бы встретиться и с ним.
С наилучшими пожеланиями искренне Ваш Роджер Г.Бейтс, руководитель отдела электрохимического анализа Национального бюро стандартов. (Архив академика М. М. Шульца)
В 1968 г. было осуществлено первое издание книги Р.Бейтса на русском языке (под редакцией проф. Б. П. Никольского и проф. М. М. Шульца): Determination of pH. Roger G. Bates, National Bureau of Standards. John Wiley & Sons Inc. New York — London — Sydney. 1964