Содержание:
Синонимы: инфаркт миокарда без подъема сегмента ST, нетрансмуральный инфаркт, инфаркт миокарда (ИМ) без зубца Q.
По электрокардиографическим признакам инфаркт миокарда (ИМ) делят на два типа. При одном типе на ЭКГ отмечается подъем сегмента ST (ИМпST), при другом типе, на долю которого приходится примерно 30-40% всех случаев ИМ, подъем сегмента ST отсутствует (ИМбпST).
• При инфаркте миокарда без подъема сегмента ST (ИМбпST) речь идет обычно о легкой форме заболевания, на долю которой приходится примерно 30-40% случаев ИМ.
• В острой стадии возможен незначительный подъем сегмента ST или незначительная его депрессия. Зубец Т отрицательный и обычно очень глубокий, зубец Q не определяется.
• В хронической стадии описанные изменения сегмента ST исчезают, а отрицательный зубец Т становится менее глубоким.
• При инфаркте миокарда без подъема сегмента ST (ИМбпST) возможно поражение как передней стенки ЛЖ (отведения V2-V6), так и задней (отведения II, III, aVF).
• В диагностике инфаркта миокарда без подъема сегмента ST (ИМбпST) важную роль наряду с изменениями ЭКГ играют результаты исследования сывороточных маркеров некроза миокарда: появление тропонина в крови и повышение активности креатинкиназы и ее МВ-фракции.
Патофизиология. В основе патофизиологических механизмов инфаркта миокарда без подъема сегмента ST (ИМбпST) лежит частичный некроз стенки желудочка, обусловленный субтотальным стенозом коронарной артерии в результате кровоизлияния в атеросклеротическую бляшку и последующего тромбоза просвета. Прогноз при ИМбпST более благоприятный, чем при ИМбпST, так как речь идет только о частичном некрозе стенки желудочка сердца.
Симптомы. Основным клиническим проявлением и в этом случае является сильный приступ сжимающей загрудинной боли. Тахипноэ, появление III тона и предсердного тона при аускультации сердца, а также мелкопузырчатых хрипов над легочными полями указывают на левожелудочковую недостаточность и ассоциированы с плохим прогнозом.
Диагностика инфаркта миокарда без подъема сегмента ST
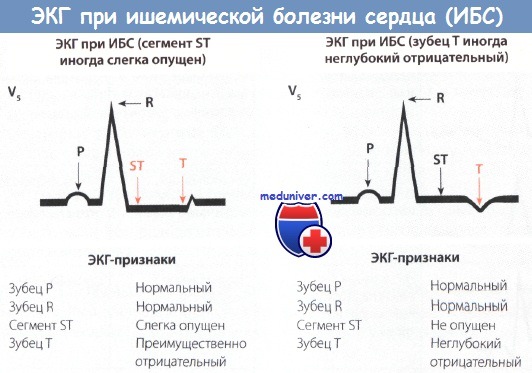
Для электрокардиографической картины инфаркта миокарда без подъема сегмента ST (ИМбпST) характерны отсутствие как отчетливого подъема сегмента ST (монофазная деформация), так и зубца Q, обусловленное некрозом миокарда.
На ЭКГ обычно выявляют незначительную или выраженную депрессию сегмента ST и отрицательный зубец Т. Подъем сегмента ST иногда бывает незначительным и быстро проходит. Глубокий отрицательный зубец Т без появления зубца Q иногда в течение нескольких дней полностью или почти полностью исчезает. Возможно, что в этом случае острая ишемия миокарда проходит в результате спонтанного тромболизиса.
В то же время отрицательные зубцы Т могут исчезать медленно, т.е. становясь все менее глубокими. Однако в обоих случаях характерный для ИМ зубец Q не выявляется.
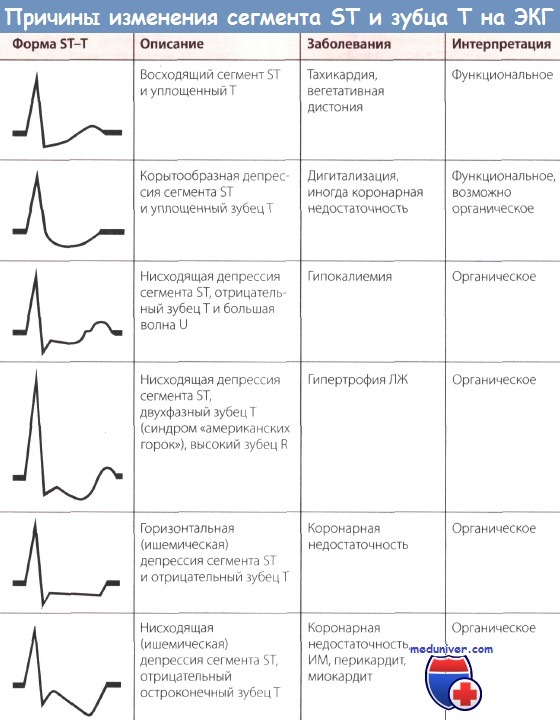
Таким образом, динамика изменений интервала ST отражает динамику событий, протекающих в просвете коронарной артерии.
Инфаркт миокарда без подъема сегмента ST (ИМбпST) может локализоваться как в передней, так и в задней стенке ЛЖ. Если пораженной оказывается передняя стенка, изменения регистрируются в отведениях V2-V6, если же задняя, то в отведениях II, III, aVF.
Поскольку описанные выше изменения могут наблюдаться и при других сердечно-сосудистых заболеваниях, например при инсульте, травме сердца, миокардите и перикардите, то для установления диагноза ИМ, помимо клинических данных, таких как длительная загрудинная боль, необходимо также, чтобы результаты исследования крови на маркеры некроза миокарда были положительными. При ИМбпST в сыворотке крови обнаруживаются тропонины и может быть повышена активность креатинкиназы.
Следует отметить ряд важных изменений, которые произошли в клинической концепции ИМ. Раньше полагали, что инфаркт миокарда без подъема сегмента ST (ИМбпST) является трансмуральным, т.е. поражает всю толщу миокарда желудочковой стенки. Поэтому считалось, что для диагностики ИМпST необходимо появление зубца Q. Поэтому ИМ с депрессией сегмента ST и глубоким отрицательным зубцом Т, но без зубца Q трактовали как нетрансмуральный инфаркт (или рудиментарный инфаркт). Эта точка зрения оказалась ошибочной.
Сегодня на основании сравнения клинических и патологоанатомических наблюдений стало известно, что иногда ИМ, проявляющийся на ЭКГ глубоким зубцом Q, может оказаться нетрансмуральным. Кроме того, показано также, что при нетрансмуральном ИМ могут появиться также глубокие зубцы Q, хотя инфаркт может охватывать только 10-20% толщины желудочковой стенки. Таким образом, наличие патологического зубца Q на ЭКГ при трансмуральном ИМпST не обязательно.
Тем не менее по статистике при трансмуральном ИМ зубец О на ЭКГ регистрируется чаще (примерно в 70% случаев), чем при нетрансмуральном ИМ (примерно в 30% случаев).
Дальнейшая тактика:
• после коронароангиографии при необходимости выполняют ЧКВ со агентированием стенозированной артерии или коронарное шунтирование
• системный тромболизис
Особенности ЭКГ при инфаркте миокарда без подъема сегмента ST (нетрасмурального инфаркта):
• частичный некроз миокарда желудочковой стенки, обусловленный стенозом коронарной артерии
• сильная сжимающая загрудинная боль
• ЭКГ: глубокий отрицательный зубец Т
• отсутствие зубца Q
• положительный результат анализа крови на тропонины, а также креатинкиназу и ее МВ-фракцию
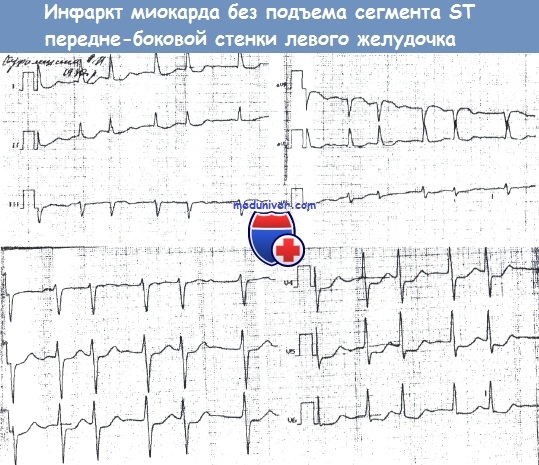 Трактовка ЭКГ. Имеется депрессия сегмента ST в отведениях I, avL, V2-V6.
Трактовка ЭКГ. Имеется депрессия сегмента ST в отведениях I, avL, V2-V6.
Главным симптомом, который запускает последовательность диагностических и лечебных мероприятий у пациентов с подозрением на острый коронарный синдром является боль в грудной клетке. Ангинозная боль — ощущение сильного сжатия и тяжести за грудиной и/или в эпигастральной области. Боль обычно иррадиирует (отдает) в левую руку, левое плечо, лопатку, шею. Реже — в обе руки и плечи, межлопатковое пространство, нижнюю челюсть, эпигастральную область. Иногда боль может иррадиировать только в правую руку и плечо, иногда в левую ногу, яичко. Боль бывает интенсивный — «кинжальний», раздирающий, жгучий. Болевые ощущения протекают волнообразно, периодически уменьшаясь, но не прекращаются полностью. Часто боль сопровождается чувством беспокойства, возбуждения, страхом смерти. Начало боли внезапное, длится от 20 минут и больше. Прием препаратов нитратов не снимает боль полностью, но может его ослабить. У пациентов старшего и пожилого возраста, женщин и больных сахарнім диабетом типичный ангинозный боль наблюдается редко. Могут наблюдаться абдоминальный (боль в эпигастральной области, тошнота, рвота, вздутие живота), аритмичный (перебои в ритме сердца, тахикардия, слабость), цереброваскулярний (головная боль, головокружение, потеря сознания), астматический (одышка, кашель) варианты. Встречается также бессимптомная форма, которая может проявляться быстрой утомляемостью, слабостью, учащенным сердцебиением, чувством страха и беспокойством.
Согласно данных электрокардиографии выделяют две группы пациентов:
- Пациенты с острой болью в грудной клетке и подъемом сегмента ST на ЭКГ, продолжается более 20 мин – острый коронарный синдром с подъемом сегмента ST, что в большинстве случаев свидетельствует о полную окклюзию (закрытие) одной или более коронарных артерий и почти всегда приводит к развитию острого инфаркта миокарда с подъемом сегмента ST — STEMI;
- Пациенты с острой болью в грудной клетке, но без длительного подъема сегмента ST на ЭКГ. При чем, картина возможных изменений на ЭКГ включает не только подъем, но и депрессия (снижение) сегмента ST, инверсию зубца Т, его уплощение или псевдонормалізацію. Иногда, изменения на ЭКГ вообще отсутствуют. Такое состояние называется острым коронарным синдромом без подъема сегмента ST и у большинства пациентов может приводить к развитию острого инфаркта миокарда без подъема сегмента ST — NSTEMI.
Клинические проявления острого NSTEMI инфаркта миокарда имеют очень широкий спектр: от бессимптомного течения до развития нестабильной гемодинамики (снижение артериального давления) – кардиогенного шока и даже остановки сердца.
В связи с тем, что объем миокарда, который погибает в результате ишемии (прекращения кровоснабжения) увеличивается очень быстро (это, в свою очередь, может привести к развитию злокачественной желудочковой аритмии) основой лечения таких пациентов является быстрое проведение диагностической коронарной ангиографии с восстановлением кровотока по коронарным сосудам.
Диагностика
Физикальное обследование больных на острый инфаркт миокарда без подъема сегмента ST часто не выявляет значительных особенностей. Вместе с этим могут наблюдаться признаки сердечной недостаточности, шоке, электрической нестабильности, что ускоряет необходимость проведения диагностических вмешательств и проведения лечения. Иногда, обнаруживают систолический сердечный шум, что свидетельствует о развитии механических осложнений инфаркта миокарда (отрыв папиллярных мышц или разрыв межжелудочковой перегородки).
Опыт специалистов клиники EuReCa уже на этапе физикального обследования может выявить другие причины развития боли в грудной клетке и изменений на ЭКГ: тромбоэмболии ветвей легочной артерии, мио-, перикардит, аортальный стеноз, пневмонии, пневмоторакс и др.
Обследование пациентов с острым инфарктом миокарда без подъема сегмента ST (или с острым коронарным синдромом без подъема сегмента ST) включает:
- проведение электрокардиографии в 12 отведениях
- определение уровня тропонина – основного и наиболее чувствительного биомаркера повреждения миокарда
- проведение трансторакальной Эхо-кардиографии
- проведение диагностической коронароангиографии
Определение уровня тропонина имеет преимущества с точки зрения точности обнаружения гибели кардиомиоцитов, сравнительно с такими маркерами, как креатинкиназа (и ее МВ-фракция) и миоглобин. Вместе с этим, не редко существует потребность в определении сразу нескольких биомаркеров, особенно при позднем обращении пациента, для определения времени начала ишемии, дальнейшей тактики лечения и его эффективности.
Необходимо отметить, что в подавляющем большинстве случаев рост уровня тропонина обусловлен повреждением миокарда, но наличие где-либо состояний (тахиаритмии, сердечная и почечная недостаточность, шок, сепсис, миокардиты, тромбоэмболия легочной артерии, расслоение аорты, рабдомиолиз, инфильтративные заболевания – амилоидоз, гемохроматоз, слеродермия, гипо — и гипертиреоз) приводит к его повышению, что не связано с гибелью кардиомиоцитов.
Пациентам, у которых отсутствуют изменения на ЭКГ, свидетельствующие о ишемию миокарда и отрицательным тестом определения уровня тропонина, которые в течение нескольких часов не чувствуют боли необходимо проведение стресс-проб на выявление пришествиеванного ишемии. Согласно Европейским рекомендациям стресс- Эхокг с фармакологическими пробами имеет преимущества с точки зрения точности диагностики и безопасности перед ЭКГ пробами с физической нагрузкой.
Согласно действующих рекомендаций в клинике EuReCa применяется алгоритм, который включает количественную оценку риска ишемии миокарда основанную на шкале GRACE. Такой подход имеет доказанные преимущества по сравнению, как с обычной клинической оценке состояния пациента, так и применение шкалы TIMI.
Лечение
Медикаментозная терапия
Целью противоишемичной терапии является обеспечение потребностей миокарда в кислороде, что достигается назначение оксигенотерапии (пациентам с насыщением крови кислородом 90% и меньше или с одышкой), нитратов, бета-блокаторов. Если такое лечение не приводит к быстрому исчезновению симптомов ишемии, то таким пациентам, независимо от изменений на ЭКГ и уровня тропонинов крови, показано проведение обезболивания и экстренной диагностической коронароангиографии.
Необходимо отметить, что применение нитратов не допустимо у пациентов, которые в течение предыдущих суток принимали ингибиторы фосфодиэстеразы 5 типа (силденафил, тадалафил или варденафил).
Применение бета-блокаторов уменьшает потребность миокарда в кислороде и является полезным для большинства пациентов, не имеющих противопоказаний к их применению. Вместе с этим, их применение у пациентов с высоким риском развития кардиогенного шока (возраст 70 лет и более, часто сердечных сокращений 110 ударов в минуту и выше и уровень систолического артериального давления менее 120 мм рт.ст.) приводит к росту частоты развитие кардиогенного шока и смерти. Итак, на сегодняшний день не рекомендовано применение бета-блокаторов у пациентов с острым инфарктом миокарда без подъема сегмента ST и с неизвестной функцией левого желудочка (которая определяется по данным Эхокг) и у пациентов с подозрением на спастические (спазм коронарных артерий) механизм развития ишемии.

GRACE = Global Registry of Acute Coronary Events challenge (Глобальный регистр острых коронарных событий);
hs-cTn = high sensitivity cardiac troponin (высокочувствительный сердечный тропонін);
ULN = upper limit of normal, 99 th percentile of healthy controls (верхняя граница нормы, 99% здоровых людей).
∆ изменение, в зависимости от анализа. Высокое ненормальное hsTn определяет пятикратное превышение нормального.
Рисунок 1. Алгоритм диагностики острого коронарного синдрома без подъема сегмента ST.
У пациентов последней группы необходимо применять блокаторы кальциевых каналов группы дилтиазема или верапамила, которые продемонстрировали такую же эффективность в уменьшении симптомов ишемии, как и бета-блокаторы.
Пациентам с окклюзией (закупоркой тромбом) коронарных сосудов вследствие атеросклероза коронарных сосудов, как причина развития острого инфаркта миокарда без подъема сегмента ST показано применение антиагрегантов – лекарственных средств, которые уменьшают способность тромбоцитов образовывать тромбы, то есть предотвращают свертывание крови.
Применение двойной антиагрегантного терапии, включающей ацетилсалициловую кислоту и клопидогрель является наиболее эффективным. Прасугрель ингибирует активность тромбоцитов в большей степени, чем клопидогрель, поэтому не должен применяться у пациентов с высоким риском развития кровотечений. Также применение прасугрелю и тикагрелора не рекомендовано у пациентов с выраженным нарушением функции почек.
При назначении лечения специалисты клиники EuReCa обязательно рассчитывают риск развития кровотечений с использованием, согласно действующих рекомендаций, шкалы CRUSADE.
Прекращение антиагрегантного терапии несет большие риски связаны с рецидивом заболевания. Например, прекращение двойной антиагрегантного терапии после стентирования коронарных артерий достоверно увеличивает риск тромбоза стента, особенно в первой месяц прісля прекращения приема препаратов. Рекомендованная продолжительность применения двойной антиагрегантного терапии на сегодня составляет 1 год с последующим применение ацетилсалициловой кислоты. При этом, продолжительность терапии не зависит от типа стента или метода реваскуляризации миокарда.
В остром периоде лечения инфаркта миокарда без подъема сегмента ST антикоагулянта проводят терапию с применением нефракціонованого гепарина, низкомолекулярных гепаринов, фондапарінуксу или бивалирудина. Выбор конкретного препарата зависит, как от его особенностей, так и от особенностей клинической ситуации: риска развития кровотечения, функции почек, возраста и сопутствующих заболеваний, которые есть у пациента.
После завершения острой фазы при решении вопроса о применении длительной антикоагулятної терапии в клинике EuReCa используют индивидуализированный подход, который учитывает особенности каждого пациента и зависит от риска развития тромбоэмболических осложнений (которые определяются по шкале CHA2DS2-VASc) и риска развития кровотечения (шкала HAS-BLED)
Хирургическое лечение
Проведение ангиографии коронарных сосудов и, при наличии показаний, дальнейшей реваскуляризации играет центральную роль в лечении пациентов с острым инфарктом миокарда без подъема сегмента ST и, в развитых странах, проводится подавляющему большинству пациентов, обратившихся по поводу этого заболевания.
В клинике EuReCa при принятии решения о целесообразности проведения коронароангиографии мультидисциплинарная команда внимательно оценивает риски связанные с этим инвазивным вмешательства и пользу, которую можно ожидать от ее проведения.
Существуют два метода хирургического лечения острого инфаркта миокарда без подъема сегмента ST: чрескожное коронарное вмешательство и операция коронарного шунтирования. Оба метода имеют свои преимущества и недостатки, которые касаются как немедленных эффектов лечения, так и отделенных результатов и обязательно берутся во внимание специалистами для того, что бы рекомендовать их пациенту.
Скорейшее проведение коронарографии рекомендовано при наличии следующих факторов: нестабильность гемодинамики или кардиогенный шок, ангинозная боль, которая не исчезает при медикаментозном лечении, остановка сердца или развитие аритмий, угрожающих жизни, механические осложнения острого инфаркта миокарда, развитие острой сердечной недостаточности, периодический, хоть и не продолжительный подъем сегмента ST. В таких случаях проведение вмешательства желательно в течение 2-х часов от появления симптомов (немедленная инвазивная стратегия).
Коронарография в течение ближайших 24 часов (ранняя инвазивная стратегия) проводится пациентам с острым коронарным синдромом без подъема сегмента ST в случае повышения уровня тропонина, которое соответствует инфаркту миокарда, появлением новых изменений на ЭКГ или с количеством баллов по шкале GRACE более 140.
В течение 72 часов от появления симптомов (инвазивная стратегия) рекомендовано проведение коронароангиографии больным сахарным диабетом, с нарушением функции почек, фракцией выброса 40% и менее или с застойной сердечной недостаточностью, пациентам, которым ранее проводились чрескожные коронарные вмешательства или операции коронарного шунтирования или за больным с количеством баллов по шкале GRACE 110-139.
Во всех других случаях решение о проведении кронарографии принимается индивидуально и часто может быть заменено неинвазивными методами обследования.
Рутинное применение инвазивной стратегии – проведение кронарографії с последующим определением показаний для проведения реваскуляризации – рекомендуемый подход наиболее часто применяется во всем мире.
Чрескожное коронарное вмешательство при остром инфаркте миокарда без подъема сегмента ST, и при других формах атеросклероза коронарных артерий, включает проведение баллонной ангиопластики (для разрушения атеросклеротической бляшки и обеспечения проходимости венечной артерии) и стентирование пораженного участка, что значительно уменьшает вероятность ее рестенозу (повторному образованию бляшки) и тромбоза.
При остром инфаркте миокарда без подъема сегмента ST наиболее распространенным в мире сегодня является проведение полной (то есть стентирование всех пораженных сосудов) ранней реваскуляризации. Это обусловлено результатами исследований, которые свидетельствуют о вреде связанную с неполной реваскуляризацией и задержкой в проведении чрезкожного коронарного вмешательства (стентирование).
Около 10% пациентов госпитализированных с диагнозом острый коронарный синдром без подъема сегмента ST требуют проведения операции коронарного шунтирования. Как правило, чрескожное коронарное вмешательство возможно провести быстрее, чем коронарное шунтирование, но при поражении многих сосудов коронарное шунтирование обеспечивает более полную реваскуляризацию (восстановления кровоснабжения) миокарда.

Патогенез инфаркта миокарда
Инфаркт миокарда происходит из-за разрыва или надрыва атеросклеротической бляшки в коронарной артерии. При разрыве фиброзной покрышки атеросклеротической бляшки субэндотелиальная соединительная ткань соприкасается с форменными элементами крови, что ведет к активации тромбоцитов, образованию тромбина и тромбозу.
Это динамический процесс, в котором друг друга сменяют окклюзия, субтотальный стеноз и восстановление кровотока. Тромботическая окклюзия коронарной артерии при неразвитых коллатеральных артериях обычно приводит к инфаркту миокарда с подъемом сегмента ST. Патогенез инфаркта миокарда с подъемом сегмента ST и без такового в общем схожи, поэтому само по себе отсутствие подъема сегмента ST еще не означает, что объем поражения миокарда невелик.
ОКСпST ЭКГ – как правило, следствие окклюзирующего тромбоза КА. Тромб
возникает чаще всего на месте разрыва так называемой ранимой
(нестабильной) атеросклеротической бляшки (А)Б с большим липидным ядром,
богатой воспалительными элементами и истонченной покрышкой, однако
возможно образование окклюзирующего тромба и на дефекте эндотелия
(эрозии) КА над АБ. В большинстве случаев окклюзия развивается в месте
гемодинамически незначимого стеноза КА.
В КА больных с ОКС обычно находят несколько ранимых АБ, в т.ч.
имеющих надрывы. Из-за высокого риска возникновения повторных окклюзий
КА при лечении этих больных локальные воздействия в области АБ,
обусловившей развитие клинической картины ОКС, должны комбинироваться с
общими лечебными мероприятиями, направленными на снижение вероятности
тромбоза.
Тромб может быть источником эмболий в дистальное сосудистое русло
сердца. Эмболизация микрососудов миокарда сама по себе может приводить к
образованию мелких очагов некроза. Кроме того, мелкие эмболы
препятствуют восстановлению кровоснабжения миокарда (реперфузии) после
устранения окклюзии крупной КА.
Следствием ИМ является процесс ремоделирования сердца. Образование
очага некроза в миокарде сопровождается изменение размера, формы и
толщины стенки ЛЖ, а сохранившийся миокард испытывает повышенную
нагрузку и подвергается гипертрофии. Насосная функция изменившего форму
ЛЖ ухудшается, и это способствует развитию СН. Наиболее выраженная форма
ремоделирования ЛЖ при обширных ИМ связана с образованием аневризмы
стенки ЛЖ.
В последнее время предложено различать и другие типы ИМ, отличающиеся механизмами развития (Приложения Г1, Г2 и Г3).
Приложение Г4. Причины повышения уровня сердечных тропонинов в крови.
Повреждение кардиомиоцитов, связанное с первичным (спонтанным) острым нарушением коронарного кровотока
- Разрыв атеросклеротической бляшки
- Образование тромба в просвете коронарной артерии
Повреждение кардиомиоцитов, связанное с ишемией миокарда,
возникшей из-за повышения потребности миокарда в кислороде и/или
уменьшения его доставки к миокарду
- Тахи- или брадиаритмии, блокада сердца.
- Расслоение аорты или тяжелый порок аортального клапана.
- Гипертрофическая кардиомиопатия.
- Кардиогенный, гиповолемический или септический шок.
- Тяжелая дыхательная недостаточность.
- Выраженная анемия.
- АГ
- Спазм коронарной артерии.
- Эмболия в коронарную артерию или васкулит.
- Дисфункция эндотелия коронарных артерий без существенного обструктивного коронарного атеросклероза.
Повреждение кардиомиоцитов, не связанное с ишемией миокарда
- Травма сердца (контузия, операция, абляция, ЭС, разряды дефибриллятора и пр.).
- Воспалительные заболевания (миокардит, вовлечение миокарда при эндокардите или перикардите).
- Кардитоксическое воздействие лекарств и токсинов.
Повреждение миокарда вследствие нескольких причин или неустановленной этиологии
- СН (острая и хроническая).
- Стрессорная кардиомиопатия (Такоцубо).
- Тяжелая ТЭЛА или ЛГ.
- Сепсис и крайне тяжелое состояние больного.
- Почечная недостаточность.
- Тяжелое острое неврологическое заболевание (например, инсульт, субарахноидальное кровоизлияние).
- Инфильтративное заболевание (амилоидоз, гемохроматоз, саркоидоз, склеродермия).
- Обширные ожоги.
- Очень интенсивная ФН.
Многие факторы риска развития инфаркта миокарда поддаются изменениям и, таким образом, во многих случаях их можно предотвратить.
1.4. Кодирование по МКБ-10
Острый инфаркт миокарда (I21)
I21.0 – Острый трансмуральный инфаркт миокарда передней стенки
I21.1 – Острый трансмуральный инфаркт миокарда нижней стенки
I21.2 – Острый трансмуральный инфаркт миокарда других уточненных локализаций
I21.3 – Острый трансмуральный инфаркт миокарда неуточненной локализации
I21.4 – Острый субэндокардиальный инфаркт миокарда
I21.9 – Острый инфаркт миокарда неуточненный
Повторный инфаркт миокарда (I22)
I22.0 – Повторный инфаркт миокарда передней стенки
I22.1 – Повторный инфаркт миокарда нижней стенки
I22.8 – Повторный инфаркт миокарда другой уточненной локализации
I22.9 – Повторный инфаркт миокарда неуточненной локализации