ВЕНОЗНЫЕ ТРОМБОЭМБОЛИЧЕСКИЕ ОСЛОЖНЕНИЯ
Венозные тромбоэмболические осложнения (ВТЭО), к которым относят тромбоз глубоких вен (ТГВ), тромбоз подкожных вен (ТПВ, тромбофлебит) и тромбоэмболию легочных артерий (ТЭЛА), на протяжении многих десятилетий остаются важнейшей клинической проблемой, которая касаетсяпациента с любой патологией и врачей всех специальностей.
Тромботическое поражение венозного русла нижних конечностей, прежде всего, глубоких вен, является острым состоянием, развивающимся в результате комплексного действия ряда факторов. Ежегодно в общей популяции на каждую 1000 человек регистрируется 1,2-1,4 случая ТГВ и 0,5-0,6 случаев ТЭЛА. При этом частота ВТЭО возрастает с возрастом достигая значения 5 случаев на 1000 человек ежегодно у лиц старше 80 лет. Каждый год в станах Евросоюза регистрируется около 1 миллиарда эпизодов ВТЭО, треть из которых представляет собой смертельную легочную эмболию. Экстраполяция этих данных на население Российской Федерации свидетельствует о том, что ежегодно когорта «венозных» пациентов в нашей стране увеличивается на 90-100 тыс.
Непосредственная угроза жизни больного связана не с тромботическим поражением венозного русла, а с ТЭЛА. В течение месяца после выявления ТГВ от нее умирает 6% пациентов. После перенесенной легочной эмболии летальность в первые несколько месяцев может достигать 17,4%. Но даже благополучный исход острого периода не означает исчезновения проблемы. В отдаленном периоде после тромбоза глубоких вен формируется посттромботическая болезнь (ПТБ) нижней конечности, сопровождающаяся глубокой дезорганизацией работы венозной системы нижних конечностей с высокой вероятностью развития трофических язв при отсутствии адекватного лечения. Еще одним возможным осложнением ТЭЛА служит хроническая постэмболическая легочная гипертензия (ХПЭЛГ), развивающаяся в исходе распространенной обструкции легочного артериального русла. Тяжелая ХПЭЛГ в течение 5 лет приводит к смерти 10-15% больных, перенесших массивную ТЭЛА.
Отдельно стоит проблема внутригоспитальных ВТЭО. Среди госпитализированных пациентов частота венозных тромбоэмболий возрастает более чем в 100 раз и наблюдает с частотой 96 случаев на 1000 госпитализированных пациентов ежегодно. Не смотря на активное развитие и внедрение методов профилактики ВТЭО, их госпитальная частота за последние десятилетия не только не снижается, но и возросла для ТГВ в 3,1 раза, для ТЭЛА — в 2,,5 раза.
- Венозные тромбоэмболические осложнения – собирательное понятие, объединяющее тромбоз подкожных, глубоких вен, а так же легочную тромбоэмболию.
- Тромбоз глубоких вен – наличие тромба в глубокой вене, который может вызвать ее окклюзию.
- Тромбоз подкожных вен (тромбофлебит) – наличие тромба в подкожной вене, которое обычно сопровождается клинически определяемым воспалением.
- Тромбоэмболия легочных артерий — (легочная тромбоэмболия, легочная эмболия) – попадание в артерии малого круга кровообращения тромбов–эмболов, которые мигрировали из вен большого круга.
- Посттромботическая болезнь – хроническое заболевание, обусловленное органическим поражением глубоких вен вследствие перенесенного тромбоза. Проявляется нарушением венозного оттока из пораженной конечности.
- Хроническая постэмболическая легочная гипертензия – патологическое состояние, вызванное хронической окклюзией или стенозом легочного артериального русла после тромбоэмболии легочных артерий, чреватое развитием хронического легочного сердца.
Механизм прижизненного образования тромбов внутри сосудов описывается триадой, открытой в 1856 году немецким морфологом Рудольфом Вирховым, которая включает в себя повреждение сосудистой стенки, замедление кровотока и повышенную вязкость (свертывающую способность) крови.
Наиболее значимыми для возникновения венозного тромбоза является гемодинамические нарушения (замедление кровотока) и гиперкоагуляция (повышенная свертываемость крови). В этих условиях ключевую роль в формировании тромба играет активация процессов свертывания крови, приводящая к образованию фибрина.
Вероятность венозного тромбоза увеличивается, если у человека имеется врожденная или приобретенная тромбофилия — т.е. состояние, характеризующееся склонностью к тромбо бразованию вследствие дефицита естественных антикоагулянтов. С наличием тромбофилии могут быть связаны многие случаи “неожиданного” венозного тромбоза и легочной тромбоэмболии (в частности, возникающие у лиц молодого возраста, не имеющих серьезных клинических факторов риска). Инициировать тромбоз у пациентов с тромбофилией могут оперативные вмешательства, травмы, беременность и роды — т.е. те состояния, которые сопровождаются повреждением тканей, изменением тонуса сосудов, гормонального фона. Высокий риск флеботромбоза существует у больных, страдающих злокачественными новообразованиями.
Повреждение венозной стенки с нарушением целостности внутренней эндотелиальной выстилки выступает важным механизмом, инициирующим тромбоз. Среди причин – прямое повреждение при установке внутрисосудистых катетеров и других устройств (фильтров, стентов и пр.), протезировании вен, травме, операции. К повреждению эндотелия приводят гипоксия, вирусы, эндотоксины. Обширные оперативные вмешательства, тяжёлые механические травмы, массивная кровопотеря, распространённые ожоги, инфекционные заболевания и сепсис включают механизм системной воспалительной реакции, заключающийся в выработке и выделении в кровоток большого числа биологически активных соединений (гистамина, серотонина, фрагментов комплемента, лейкотриенов, брадикинина, фактора релаксации сосудов). Каскад цитокинов активирует лейкоциты и способствует их адгезии к эндотелию. Выделяемые активированными лейкоцитами мощные оксиданты вызывают гибель эндотелиальных клеток с последующим обнажением субэндотелиального слоя.
Нарушение кровотока вызывается варикозным расширением вен, сдавлением сосудов извне (опухолями, кистами, воспалительными инфильтратами, увеличенной маткой, костными фрагментами), разрушением клапанного аппарата после перенесённого ранее флеботромбоза. Одной из важных причин замедления тока крови служит вынужденное пребывание в неподвижном состоянии (гипсовая иммобилизация, скелетное вытяжение, длительное авиа- или автопутешествие), что приводит к нарушению функции мышечно-венозной помпы голеней. У терапевтических больных, вынужденных соблюдать постельный режим, недостаточность кровообращения, кроме замедления тока крови, приводит к повышению венозного давления, увеличению диаметра вен, увеличению вязкости крови. Основное терапевтическое заболевание может приводить к обезвоживанию, изменению соотношения свертывающей и противосвертывающей систем крови и значительно повышать риск венозного тромбоза. Известно, что большая часть пациентов многопрофильного стационара, страдающих от ВТЭО — это пациенты терапевтического профиля.
У хирургических больных риск венозного тромбоза зависит от травматичности (обширности) и продолжительности оперативного вмешательства. Немаловажное значение имеют общее состояние пациента на момент операции, наличие сопутствующей патологии, вид анестезии, обезвоживание, а также длительность пребывания на постельном режиме.
Ведущие факторы риска развития венозного тромбоза и легочной эмболии:
Умеренно повышающие риск венозного тромбоэмболизма:
- Возраст. После 40 лет отмечается рост частоты ВТЭО, которая еще заметнее увеличивается у лиц старше 60 лет. Максимальная частота наблюдает после 80 лет.
- Избыточная масса тела и ожирение. У пациентов с избыточной массой тела отмечается повышение в крови количество прокоагулянтных факторов (ИАП-1). Также ожирение может сопровождаться нарушением толерантности к глюкозе, артериальной гипертензией, повышенным содержанием жиров в крови (гипертриглицеридемия), что рассматривается вместе как "метаболический Х-синдром" и часто характеризуется повышенной вязкостью крови и склонностью к гиперкоагуляции.
- Хроническая сердечная недостаточность 2 класса по Образцову-Строжеско; 3-4 класса по функциональной классификации Нью-Йоркской ассоциации кардиологов (NYHA). Сердечная недостаточность характеризуется значительным нарушением венозного отток от нижних конечностей, венозным застоем. Ситуацию усугубляет прием нитроперпаратов, обладающих значительным вазодилатирующим эффектом.
- Варикозная болезнь и другие хронические заболевания вен также ассоциируются с замедлением венозного оттока и стазом крови.
- Прием эстрогенсодержащих препаратов (оральная контрацепция, гормонзамещающая терапия в постменопаузальном периоде). Женские половые гормоны оказывают отрицательное влияние на тонус вен, ухудшая отток венозной крови, а также повышают когуляционную активность крови, увеличивая риск развития тромбоза.
- Прием селективных модуляторов эстрогеновых рецепторов (тамоксифен).
- Беременность и ближайший послеродовый период (6 недель) характеризуются значительными гормональными изменениями, преобладанием эстрогенов в крови, гемоконцентрацией, что приводит к значительному повышению свертывающей активности крови.
- Длительный постельный режим, иммобилизация (гипс, скелетное вытяжение) более 3 суток, длительное авиа или автопутешествие (более 8 часов) приводят к венозному застою вследствие отсутствия активности мышечно-венозной помпы голени.
- Катетеризация центральной вены сопровождается повреждением эндотелиальной выстилки сосуда и способствует образованию тромба в этом месте.
- Острые воспалительные заболевания (пневмония, колит) сопровождаются выбросом значительного количества медиаторов воспаления и факторов свертывания.
- Сдавление вен объемным образованием (чаще на уровне малого таза) приводит к значительному нарушению венозного кровотока и стазу крови.
- Прочие причины: нефротический синдром (потеря больших количеств антитромбина-3), пароксизмальная ночная гемоглобинурия (холодовой внутрисосудистый гемолиз эритроцитов), миелопролиферативные заболевания (повышенная вязкость крови из-за избытка форменных элементов).
Значительно повышающие риск венозного тромбоэмболизма:
- Онкологическое заболевание.
- Опухоли являются источником мощных прокоагуляционных факторов (тканевой тромбопластин), собственных факторов, повышающих свертываемость крови, а также в ответ на опухолевые клетки могу образовываться специфические антитела, обуславливающие прокоагуляционные сдвиги крови (паранеопластический синдром). Среди онкологических заболеваний, являющихся фоном для венозных тромбозов, чаще встречаются рак поджелудочной железы, мозга, желудка, толстой кишки, легких, предстательный железы, почек, яичника.
- Парезы и параличи вследствие нарушения мозгового (инсульт) кровообращения или травмы. Обездвиженность приводит с одной стороны к застою крови в венах голени, с другой стороны повреждение ткани мозга способствует выбросу большого количества факторов свертывания крови.
- Эпизоды ВТЭО в анамнезе.
- Тромбофилия — врожденная или приобретенная склонность к тромбообразованию, которая может носить семейный характер. Подробнее о наиболее распространенных видах тромбофилии — в соответствующем разделе.
- Сепсис — системная воспалительная реакция, характеризующаяся неконтролируемым выбросом огромных количеств воспалительных медиаторов, приводящих к нарушению функции эндотелия и его гибели, что в свою очередь расценивается организмом как повреждение сосуда и запускает коагуляционный каскад.
А.И.Кириенко, С.Г.Леонтьев, И.С.Лебедев, Е.И.Селиверстов
Кафедра факультетской хирургии РГМу (зав. — акад. В.С.Савельев), городская клиническая больница №1 им. Н.И.Пирогова (главный врач — проф. О.В.Рутковский)
Венозные тромбоэмболические осложнения (ВТЭО) — одни из самых опасных и зачастую трагических у больных хирургического профиля. Они включают тромбоэмболию легочных артерий (ТЭЛА), источником которой более чем в 90% случаев является тромбоз в системе нижней полой вены. В среднем их частота составляет 1 на 1000. Традиционно с наибольшей частотой при отсутствии профилактики (45-84%) они встречаются после протезирования тазобедренного или коленного суставов, у каждого второго больного с сочетанной травмой. Тромботические осложнения развиваются в послеоперационном периоде у 30% пациентов со злокачественными новообразованиями, в 24 и 19% случаев после нейрохирургических и общехирургических вмешательств соответственно.
Зачастую массивная ТЭЛА, летальность от которой колеблется от 0,1 до 5%, является первым проявлением бессимптомно протекающего острого флеботромбоза. Подобное течение тромбоза, по данным T.Hyers [1], в послеоперационном периоде отмечается у 80% больных. По данным патолого-анатомического отделения ГКБ №1 им. Н.И.Пирогова, массивная ТЭЛА после урологических, хирургических, гинекологических вмешательств выявляется в 7,1, 8,3 и 11,2% случаев соответственно. Кроме того, примерно половина больных с тромбозом подколенного или бедренно-подвздошного сегмента переносят бессимптомную легочную эмболию [2]. Неверифицированные тромбоэмболические осложнения угрожают возникновением в отдаленном периоде тяжелых форм хронической венозной недостаточности нижних конечностей и постэмболической легочной гипертензии, что негативно отражается на качестве жизни и требует существенных финансовых затрат на их лечение. В связи с этим вопросы профилактики тромбоэмболических осложнений у хирургических больных по-прежнему актуальны.
Приведенные данные заставляют клинициста ответить на вопрос: какова вероятность развития венозного тромбоза и легочной эмболии у данного конкретного больного? Для этого необходимо провести анализ совокупности факторов риска, предрасполагающих к возникновению ВТЭО в послеоперационном периоде. Они обусловлены, с одной стороны, оперативным вмешательством, а с другой — характером патологии (в том числе и сопутствующей), имеющейся у пациента. Риск осложнений в наибольшей степени зависит от типа операции и ее продолжительности. Выделяют неосложненные вмешательства (длительностью от 30 до 45 мин), большие и расширенные. К первым относят аппендэктомию, грыжесечение, выскабливание полости матки, гистероскопию, трансуретральную резекцию предстательной железы, диагностическую лапароскопию и эндоскопические операции и т.д. Глубоким заблуждением является мнение, что они никогда не сопровождаются ВТЭО. Так, у этой категории больных, частота тромбоза глубоких вен голени достигает 2%, проксимальных форм тромбоза — 0,4%, легочная эмболия развивается у 0,2% больных с летальным исходом в 0,002% случаев [3]. Венозный тромбоз и ТЭЛА регистрируются после лапароскопической холецистэктомии у 0,03 и 0,06% пациентов соответственно [4].
Из больших вмешательств, при которых чаще возникает тромбоз в системе нижней полой вены, выделяют: осложненную аппендэктомию, холецистэктомию, резекцию желудка или кишечника по поводу заболеваний неопухолевой этиологии, кесарево сечение, ампутацию матки, удаление придатков, чреспузырную аденомэктомию, гипсовую иммобилизацию или остеосинтез переломов костей голени и др. Серьезной проблемой остается отсутствие должных профилактических мероприятий после оперативного родоразрешения.
К расширенным вмешательствам, после которых частота тромбоза дистальной локализации достигает 40-80%, проксимальной — 20%, а легочная эмболия развивается у 4-10% больных, относят операции, выполняемые по поводу злокачественных новообразований любой локализации, ортопедические или травматологические (остеосинтез бедра, эндопротезирование коленного либо тазобедренного суставов). Высокая вероятность развития венозного тромбоза у этих больных обусловлена, с одной стороны, наличием онкопатологии — одного из основных самостоятельных факторов риска, а с другой — продолжительностью и объемом вмешательства, длительной иммобилизацией как до, так и после операции.
Количество факторов, связанных с состоянием пациента и влияющих на частоту ВТЭО, огромно. К основным можно отнести: возраст, наличие в анамнезе онкологических заболеваний, эпизодов венозного тромбоза и легочной эмболии, длительный (4 дня и более) постельный режим, ожирение, варикозное расширение вен нижних конечностей, прием гормональных контрацептивов, наследственные либо приобретенные тромбофилические состояния. Нередко именно сопутствующая патология при прочих равных условиях существенно увеличивает риск появления острого венозного тромбоза. Например, в старшей возрастной группе, частота тромбоэмболических осложнений в 3-4 раза выше, чем у пациентов 40-50 лет. Тот факт, что оральные контрацептивы, увеличивая содержание фибриногена в плазме крови, а также таких факторов свертывания, как протромбин, VII, IX, X, XII, повышают риск тромбозов, не вызывает сомнения. Таким образом, пациенты могут быть разделены на группы с низким, умеренным или высоким риском возникновения венозного тромбоза. Выбор методов профилактики должен проводиться соответственно степеням риска.
Постулат о том, что осложнения легче предотвратить, чем лечить, общеизвестен. В связи с этим необходимо особо подчеркнуть, что предупредить развитие венозного тромбоза означает тем самым обезопасить пациента от угрожающей его жизни легочной эмболии. Согласно триаде Вирхова активация процесса свертывания крови происходит в результате изменения ее свойств (гиперкоагуляция), повреждения сосудистой стенки, замедления тока крови (стаз). Основой профилактики служат методы, направленные на коррекцию этих нарушений, предотвращение развития острого венозного тромбоза. Их подразделяют на медикаментозные (фармакологические) и физические (механические).
Физические методы профилактики должны быть использованы у всех без исключения больных в интра- и послеоперационном периоде вплоть до полной активизации. Они включают эластическую компрессию нижних конечностей и перемежающуюся пневмокомпрессию. При этом наблюдается уменьшение венозной емкости нижних конечностей, улучшение скоростных и вязкостных характеристик крови. Методы ускорения кровотока особенно эффективны у нейрохирургических больных, у пациентов с сочетанной травмой, когда проведение фармакопрофилактики равносильно "катастрофе" из-за риска геморрагических осложнений. Так, например, периоперационная переменная пневмокомпрессия в нейрохирургии снижает частоту развития венозного тромбоза с 22 до 7% [3]. Немаловажную роль играет и уровень компрессии, особенно у пациентов высокой степени риска. По данным A.Howard и соавт. (2004 г.), компрессия всей конечности снижает частоту развития тромбоза в 2,5 раза (см. таблицу). Не следует забывать, что одной из составляющих немедикаментозной профилактики ВТЭО служит максимальная и возможно более ранняя активизация больных, перенесших хирургические вмешательства. В этой связи необходимо отметить преимущества регионарной анестезии над общей в снижении частоты этих осложнений, особенно у травматологических и ортопедических больных.
Таблица. Влияние уровня компрессии на частоту возникновения послеоперационных тромбозов
| Длина компрессионного трикотажа | Частота возникновения венозного тромбоза | ||
| низкий риск, % | умеренный риск, % | высокий риск, % | |
| Компрессия до колена | 0 | 0 | 8,6 |
| Компрессия до паха | 0 | 0 | 3,2 |
Основным методом профилактики флеботромбоза и связанной с ним легочной эмболии у пациентов умеренного и высокого риска должна быть фармакопрофилактика. Доказанной на сегодняшний день эффективностью обладают антикоагулянты прямого и непрямого действия. Кратковременная профилактика традиционно осуществляется гепаринами различной молекулярной массы, длительная — антагонистами витамина К. В клинической практике предпочтение сегодня отдано низкомолекулярным гепаринам, преимущество и безопасность которых подтверждено многочисленными исследованиями. В плацебо-контролируемом исследовании
D.Bergqvist и соавт. [5] продемонстрировал, что применение тинзапарина у экстренных хирургических больных снижает частоту возникновения флеботромбоза с 22 до 7,7%. A.Cyrkowicz (2002 г.) при использовании надропарина, выявил уменьшение частоты тромбоза глубоких вен нижних конечностей и легочной эмболии после различных гинекологических вмешательств с 3,01 и 0,22% до 1,12 и 0% соответственно. D.Bergqvist и соавт. [6] показали, что применение эноксапарина в сравнении с нефракционированным гепарином у пациентов, оперированных по поводу злокачественных новообразований, снижает частоту возникновения тромбоза с 17,6 до 14,4%. Надропарин в сочетании с градуированной компрессией нижних конечностей у нейрохирургических больных снижает риск тромбоза глубоких вен (проксимальных форм) с 26,3% (12%) до 18,7% (7%), без увеличения частоты больших геморрагических осложнений [7].
Таким образом, широкое использование в клинической практике низкомолекулярных гепаринов у пациентов умеренного и высокого риска развития ВТЭО считают необходимым и оправданным.
Предпринимаемый комплекс профилактических мероприятий должен не только соответствовать степени риска ВТЭО, но и быть экономически оправданным. В группе низкого риска тромбоэмболических осложнений достаточно осуществлять компрессию нижних конечностей, используя эластичный бинт или специальный компрессионный трикотаж. В остальных группах, наряду с ними также целесообразна переменная пневмокомпрессия. Фармакопрофилактика показана только тем пациентам, у которых существует умеренный либо высокий риск развития острого венозного тромбоза.
Когда начинать и как длительно следует проводить фармакопрофилактику? Первую инъекцию нефракционированного либо низкомолекулярного гепарина назначают соответственно за 3-12 ч до операции, а затем повторяют через равный промежуток времени после. При высокой вероятности технических проблем во время вмешательства, опасности кровотечений, операции в экстренном порядке профилактика может быть начата через 6-12 ч после ее завершения, но не позднее этого срока, так как формирование тромба, как правило, начинается уже на операционном столе, либо тотчас после ее окончания. Нефракционированный гепарин вводят 3 раза в сутки по 5000 ЕД через каждые 8 ч, низкомолекулярные -однократно подкожно. Ориентировочные дозировки составляют при умеренном/высоком риске: эноксапарин 20/40 мг, надропарин 0,3/0,6 мл, дальтепарин 2500/5000 МЕ. Как правило, длительность фармако-профилактики составляет 7-10 дней. Между тем, у ряда больных с высокой вероятностью развития ВТЭО (травматологические повреждения, онкологические заболевания, курсы химио- и лучевой терапии) этого явно недостаточно. Им необходима пролонгированная профилактика (до 1,5 мес и более), которую проводят непрямыми антикоагулянтами под контролем международного нормализованного отношения (в пределах 2,0-3,0). У целого ряда пациентов применение антагонистов витамина К невозможно из-за наличия противопоказаний. В этих случаях целесообразно использовать профилактические дозы низкомолекулярных гепаринов.
Заслуживают особого обсуждения клинические наблюдения, когда еще до предполагаемой операции обнаруживают тромбоз в системе нижней полой вены. Наиболее часто это наблюдается у пациентов травматологического профиля, у которых флеботромбоз развивается из-за длительного постельного режима. У 10% больных венозный тромбоз служит первым проявлением злокачественных новообразований любой локализации. Таким больным показана терапия лечебными дозами антикоагулянтов и решение вопроса о необходимости хирургической профилактики ТЭЛА, так как существует высокий риск легочной эмболии в интра- и послеоперационном периоде. Арсенал средств хирургической профилактики включает как прямые (пликация нижней полой вены), так и эндоваскулярные (имплантация временных либо постоянных моделей кава-фильтров) методы. Обычно из-за меньшей травматичности преимущество отдается эндоваскулярным методам профилактики. Когда предполагается операция на органах брюшной полости, одновременно с основным вмешательством может быть выполнена пликация нижней полой вены.
Следует отметить, что стратегия профилактики ВТЭО относится не только к хирургическим больным. Она предполагает использование комплекса мер у всех госпитальных больных, а в ряде случаев и амбулаторных. Исключение из практики зачастую формального подхода к методам профилактики, разработка и внедрение новых лекарственных средств, несомненно, позволит улучшить результаты.
Список использованной литературы
- Hyers TM, Hull RD, WeisJG. Antitbrombotic therapy venom throemboembolic disease. Chest 1995; october8:335-51.
- Partch H, KechavarzB, Mostbeck A et al. Frequency of pulmonary emboltim in patients who have iliofemoral deep vein thrombosis and are treated with once- or twice-daily low-molecular-weight-heparin.J Vasc Surg 1996; 24: 774-82.
- Geerts WH, Heit JA, Clagett GP et al. Prevention of venous thromboembolism. Chest2001; 119 (suppl. 1): 132-75.
- Lindberg F, Bergqvtit D, Rasmussen I. Incidence of thromboembolic complications after laparoscopic cholecystectomy: review of the literature. Surg LaparoscEndosc 1997; 7:324-31.
- Bergqvist D, Flordal PA, Friberg B et al. Thrombo-prophylaxy with a low molecular weight heparin (tinzaparin) in emergency abdominal surgery. A double-blind multicenter trial Vasa 1996; 25: 156-60.
- ENOXACAN Study Group. Efficacy and safety of enoxaparin versus unfractionated heparin for prevention of deep vein thrombosis in elective cancer surgery: A double-blind randomized multicentre trial with venographic assessment. Br J Surg 1997; 84:1099-1003.
- Nurmohamed MT, van Riel AM, Henkens CM et al. Low molecular weight heparin and compression stockings in the prevention of venous thromboembolism in neurosurgery. Thromb Haemost 1996; 75: 233-8.
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.


Читайте в новом номере
РГМУ имени Н.И. Пирогова
В енозные тромбоэмболические осложнения (ВТЭО) превратились в последние годы в актуальнейшую медицинскую проблему. На фоне общего снижения операционной летальности венозный тромбоз и легочная эмболия становятся доминирующими послеоперационными осложнениями. Тромбоэмболия легочных артерий, в том числе и с фатальным исходом, к сожалению, не редкость в различных хирургических стационарах. Особенно угрожающим выглядит положение дел в травматологических и ортопедических отделениях, где ВТЭО отмечаются более чем у половины пациентов. Не менее тревожна ситуация в акушерстве. В экономически развитых странах эмболия легочных артерий занимает I-III места в структуре материнской смертности. Тромбоз глубоких вен нижних конечностей является также уделом многих пациентов терапевтических стационаров. По обобщенным данным, его частота у больных инфарктом миокарда составляет в среднем 24%, а при инсульте — 42%.
Не будет преувеличением сказать, что в госпитальных отделениях любого профиля без труда можно обнаружить пациентов с ВТЭО. При этом клинически диагностируемые тромбозы и эмболии зачастую представляют лишь видимую "вершину айсберга", поскольку в ряде случаев венозный тромбоз протекает бессимптомно, либо диагностируется уже после выписки больного из стационара, а статистические данные учитывают, в основном, массивную легочную эмболию, приведшую к летальному исходу.
Экономические затраты на диагностику и лечение ВТЭО значительны и имеют стойкую тенденцию к увеличению во всем мире. Кроме того, к ним необходимо приплюсовать материальные и моральные потери от длительного и не всегда успешного лечения хронической венозной недостаточности и постэмболической легочной гипертензии, инвалидизации больных, значительного снижения их социальной активности и уровня качества жизни. Классическое утверждение о том, что любую болезнь легче предупредить, чем лечить, в полной мере относится к венозным тромбозам, учитывая их широкое распространение, возможные тяжелые осложнения, серьезные последствия, экономическую и социальную значимость. Между тем эта аксиома пока не стала руководством к действию для всех врачей по отношению к ВТЭО.
Прежде чем говорить о программе профилактики ВТЭО, целесообразно остановиться на группах риска, т.е. тех пациентах, у которых реальна угроза возникновения тромбоза глубоких вен нижних конечностей. Это же определяет возможность развития эмболии легочных артерий, так как тромбоз в системе нижней полой вены служит основным ее источником.
Многочисленные клинические исследования показали, что опасность ВТЭО особенно велика у пациентов:
• в послеоперационном периоде
• с травматическими повреждениями костей и суставов
• соблюдающих постельный режим
• с генетически обусловленными тромбофилиями
• принимающих гормональные препараты, содержащие эстрогены
• беременных (особенно в III триместре) и рожениц.
В свою очередь, на вероятность развития венозного тромбоза в каждой из групп влияют многие факторы: ожирение, возраст, сопутствующие заболевания, принимаемые лекарственные препараты, приобретенные тромбофилические состояния различного генеза и пр. У оперированных больных огромное значение имеют длительность хирургического вмешательства, его объем и травматичность, локальное сдавление сосудов, вид анестезии, степень ограничения подвижности пациента в послеоперационном периоде.
Планируя профилактические мероприятия, которые подразделяют на физические (механические) и фармакологические, следует предусмотреть использование всех возможностей коррекции факторов, определяющих развитие венозного тромбоза.
В первую очередь это относится к послеоперационным тромбозам. Данные анкетирования, проведенного на IX Всероссийском съезде хирургов (Волгоград, 2000 г.), показали, что тромбоэмболии легочной артерии больше, чем кровотечения, опасаются 73% опрошенных. Вместе с тем оценку риска ВТЭО перед операцией всегда проводят лишь 47% клиницистов. Только 19% хирургов в обязательном порядке используют эластическую компрессию нижних конечностей (доступную меру предупреждения тромбоза). Обычно (73%) применение компрессии ограничивают случаями выраженного варикозного расширения вен. К профилактическому назначению антикоагулянтов при высоком риске тромбоза прибегают 63% хирургов. Весьма отрадный факт, тем более что еще несколько лет назад этот показатель не превышал 15%. Тем не менее, еще многие хирурги относятся к массивной тромбоэмболии легочных артерий, развившейся в послеоперационном периоде, как к фатальной неизбежности, не считая ее "своим" осложнением.
В Российской Федерации ежегодно производят свыше 8 миллионов операций, что дает возможность представить, сколь велика совокупность больных, подвергающихся опасности ВТЭО в связи с хирургическим вмешательством. Очевидно, что не у всех оперируемых больных опасность тромбообразования одинаково высока. Соответственно, и объем профилактических мер требуется различный. Для практических целей оправдано подразделение больных на группы низкого, умеренного и высокого риска ВТЭО, в зависимости от состояния больного и факторов, связанных с хирургической агрессией.
Необходимость профилактических мер существует у всех без исключения больных. Однако их объем должен быть адекватен клинической ситуации и экономически оправдан. Целесообразно соблюдать следующие правила:
• Способ профилактики должен соответствовать степени опасности ВТЭО — больные с высоким риском нуждаются в более высоком уровне защиты
• Необходимо избегать назначения "стандартной" профилактики — у больных с высоким риском она может оказаться недостаточной
• Не следует прибегать к антикоагулянтам при отсутствии показаний (реального риска ВТЭО), учитывая возможные осложнения
• При выборе способа профилактики ВТЭО целесообразно учитывать его стоимость и экономическую оправданность.
Меры профилактики должны быть задействованы уже в предоперационном периоде, продолжаться во время и после операции.
Перед плановой операцией эффективной и доступной мерой является активное поведение больного. На это следует обязательно обращать внимание, т.к. небольшое пространство отделения больницы резко ограничивает подвижность пациента. Целесообразно проведение лечебной физкультуры, использование простых тренажеров, частые прогулки хотя бы по коридору отделения. Больного следует заранее предупредить о крайней важности ранней активации в ближайшем послеоперационном периоде, необходимой в первую очередь для ритмичного сокращения икроножных мышц.
Активное поведение больного способствует ускорению кровотока и предупреждает венозный стаз. Этой же цели служит эластическая компрессия ног: эластические бинты или чулки, оказывающие постепенно снижающее от периферии в проксимальном направлении давление.
В группе низкого риска (не осложненные операции продолжительностью до 45 мин. у сравнительно здоровых пациентов) этих неспецифических профилактических мер у подавляющего числа больных оказывается достаточно. Превентивная антикоагулянтная терапия в таких условиях представляется неоправданной по соотношению риск/польза и экономически затратной.
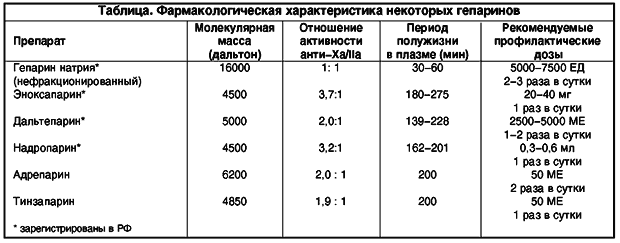
Для пациентов с умеренным риском (большие вмешательства, возраст старше 40 лет, ожирение, послеродовой период, серьезные сопутствующие заболевания) наряду с перечисленными ранее мерами возникает необходимость в профилактическом назначении антикоагулянтов. В международной клинической практике для этого используют низкомолекулярные гепарины (НМГ), важным достоинством которых по сравнению с обычным, нефракционированным гепарином (НФГ), является значительно большая длительность антитромботического эффекта после однократной подкожной инъекции (см. табл.). В профилактических целях используют малые дозы НМГ: 20 мг (0,2 мл) эноксапарина (Клексана) 1 раз в сутки под кожу живота, либо 2500 МЕ дальтепарина 1 раз в сутки либо 0,3 мл надропарина также 1 раз в сутки. Введение НМГ начинают за 2 часа до вмешательства и продолжают в той же дозе не менее 7 — 10 суток, до полной активизации больного. Используя НМГ, следует помнить, что эти препараты дозируются в совершенно иных единицах, чем обычный (нефракционированный) гепарин натрия, и не являются взаимозаменяемыми.
Применение с профилактической целью НФГ возможно, но менее желательно, поскольку он обладает существенно меньшей биодоступностью и мало предсказуемым антикоагулянтным эффектом, чаще вызывает гепарининдуцированную тромбоцитопению и остеопороз. НФГ используют в дозе 5 000 ЕД 2-3 раза в день под кожу живота.
Грубой ошибкой следует признать начало антикоагулянтной профилактики тромбоза через 2-3 дня после операции, как это иногда рекомендуется, т.к. флеботромбоз начинает развиваться раньше, зачастую уже на операционном столе. Лишь в ограниченном числе случаев, при высоком риске интраоперационного кровотечения, можно отложить введение гепарина на несколько часов. В экстренной хирургии, когда не известен коагуляционный потенциал больного, допустимо назначение антикоагулянтов после операции, но не позднее 12 часов после ее окончания.
Воздержаться от введения антикоагулянтов в этой группе пациентов целесообразно лишь при нейрохирургических и офтальмологических вмешательствах, когда даже минимальное кровотечение несет высочайшую опасность. У этих больных следует активно использовать перемежающуюся пневмокомпрессию, тренажеры икроножных мышц.
При высоком риске ВТЭО (расширенные травматические вмешательства, онкологические заболевания, необходимость длительной иммобилизации, тромбоз глубоких вен и эмболия легочных артерий в анамнезе, тромбофилии) наряду с антикоагулянтной терапией в обязательном порядке следует использовать механические меры ускорения венозного кровотока в нижних конечностях. Профилактические дозы антикоагулянтов целесообразно увеличить. В связи с этим для избежания кровоточивости во время операции первое введение НМГ можно производить за 12 часов до хирургического вмешательства. Клексан вводят по 40 мг (0,4 мл) 1 раз в сутки, дальтепарин — по 5 000 МЕ 2 раза в сутки, надропарин — по 0,4 мл первые 3 дня, затем по 0,6 мл в сутки (при массе пациента около 80 кг). Рекомендуемые дозы НФГ — 5 000-7 500 ЕД 3-4 раза в день под кожу живота. Дальнейшее увеличение количества вводимого НФГ существенно не влияет на профилактический эффект, но значительно увеличивает количество геморрагических осложнений.
Существуют еще и так называемые особые случаи, когда хирургическое вмешательство производится на фоне уже имеющегося венозного тромбоза или легочной эмболии. В такой ситуации при флотирующих, эмболоопасных тромбах выполняют имплантацию кава-фильтра или пликацию нижней полы вены, а НМГ или обычный гепарин следует использовать в лечебных дозах.
Считаем необходимым обратить внимание и на чрезвычайную важность максимально ранней активизации больного в послеоперационном периоде, продолжения использования эластической компрессии. В плановой хирургии найдется немного вмешательств, после которых (разумеется, при адекватном обезболивании) нельзя было бы поднять больного на следующие сутки и сделать с ним хотя бы десяток шагов по палате.
Серьезное значение имеет метод анестезиологического пособия. Так, использование регионарной анестезии значительно облегчает течение послеоперационного периода и в несколько раз снижает вероятность развития ВТЭО.
Все вышесказанное служит еще одним аргументом в пользу расширения практики лечения в условиях стационара одного дня, увеличения числа и круга малоинвазивных эндоскопических вмешательств.
Применяющиеся в настоящее время профилактические меры не позволяют в 100% случаев исключить формирование тромбоза в глубоких венах нижних конечностей, однако при их использовании реально минимизировать частоту тромботических осложнений, что позволяет предотвратить, по крайней мере, 2 из 3 летальных легочных эмболий. В Российской Федерации, к сожалению, систематическое профилактическое применение современных антикоагулянтов (НМГ) пока скорее исключение, чем правило. Ссылки на возможность кровотечений на фоне профилактических доз НМГ не имеют аргументированных доказательств, хотя, действительно, в 1-3% случаев возможно возникновение таких осложнений, главным образом в виде раневых гематом. Более тщательный гемостаз решает эту проблему. Вероятность кровотечений не идет ни в какое сравнение с частотой ВТЭО и тяжестью их последствий.
В ряде случаев, особенно после ортопедических операций, на фоне посттромботических изменений вен, при тромбофилиях, когда существует риск тромбообразования в отдаленном послеоперационном периоде, антикоагулянтная терапия должна быть продолжена более 7-10 дней, в том числе и после выписки больного из стационара. Для этих целей в амбулаторных условиях можно использовать НМГ, выпускаемые в форме одноразовых шприцов, удобных для выполнения инъекций самим больным. Другой вариант продолжения профилактических мер — переход на непрямые антикоагулянты (варфарин, синкумар, фенилин). Использование непрямых антикоагулянтов с профилактической целью в ближайшем послеоперационном периоде не оправдано из-за недостаточной эффективности фиксированных малых доз и высокой частоты геморрагических осложнений при использовании лечебных дозировок.
Принципы профилактики ВТЭО в травматологии сходны с таковыми у оперированных больных, поскольку в патогенезе тромбообразования очень много общего. Хочется лишь напомнить, что и без оперативных вмешательств до 10% больных старше 50 лет с переломом шейки бедра умирают от массивной ТЭЛА. Высокий риск развития венозного тромбоза после серьезных травм является основанием для антикоагулянтной профилактики. Ее начинают в течение 36 часов после травмы. Применение НМГ также является предпочтительным по сравнению с обычным гепарином, поскольку они в значительно меньшей степени вызывают остеопороз. Продолжительность использования НМГ не должна быть менее 10 дней. Наряду с этим активно используют массаж стоп и голеней, ранние движения конечностей, максимальное сокращение постельного режима. Применение перемежающейся пневматической компрессии при травмах нижних конечностей иногда невозможно или затруднено.
Беременность и роды. Во время беременности, особенно в III триместре, необходимо проводить мероприятия по борьбе с гиподинамией. Дозированные физические нагрузки, лечебная физкультура, активные прогулки перед сном служат хорошими профилактическими мерами. Улучшается венозный отток от нижних конечностей, уменьшается застой в тазовых венах. Сокращение мышц обеспечивает рост концентрации важного антитромботического фактора — тканевого активатора плазминогена. Для устранения избыточного веса следует ограничить потребление рафинированных углеводов и животных жиров.
Обязательно ношение (с I триместра) эластичных бинтов или хорошо подобранного по размеру медицинского компрессионного трикотажа I-II компрессионных классов, значительно улучшающих отток по глубоким венам и препятствующих варикозной трансформации вен подкожных с возможным развитием тромбофлебита. С той же целью рекомендуют подъем ножного конца кровати на 10-15 см. Эластическая компрессия нижних конечностей обязательна и во время родов, а также в послеродовом периоде (4-6 недель).
Немаловажным является предупреждение эмоциональных стрессов у беременных. Стрессовая реакция может вызвать активацию тромбогенного потенциала системы гемостаза и торможение фибринолиза.
Женщины, которые во время беременности перенесли венозный тромбоз, должны получать НМГ, сначала в терапевтических дозах, а затем — в профилактических, поскольку непрямые антикоагулянты им противопоказаны. Мы располагаем положительным опытом длительного применения клексана у беременных с венозным тромбозом. Поскольку антикоагулянты непрямого действия беременным противопоказаны, профилактику рецидива венозного тромбоза осуществляют с помощью длительного (фактически, до родоразрешения) использования профилактических доз гепаринов. Обязательна эластическая компрессия нижних конечностей.
После родов гепарин постепенно заменяют на антивитамины К и терапию продолжают, по крайней мере, 4-6 недель, хотя оптимальная длительность этого лечения еще не установлена. В послеродовом периоде следует рекомендовать возможно более раннюю активизацию и лечебную физкультуру.
Обсуждение вопроса о профилактике ВТЭО было бы неполным без упоминания о возможности их развития у терапевтических больных. Факторы высокого риска развития у них тромбоза во многом соответствуют перечисленным ранее. Это ожирение, длительная иммобилизация, недостаточность кровообращения, тромбоз глубоких вен нижних конечностей в анамнезе и др. Как правило, в качестве профилактики используют физические меры улучшения венозного оттока, включая посильную двигательную активность, а также дезагреганты и флеботоники. Лучший эффект дает применение НМГ (Эноксапарин (Клексан) по 40 мг в сутки, дальтепарин — по 5 000 МЕ 2 раза в сутки, надропарин — по 0,4-0,6 мл в сутки). Использование препаратов, содержащих эстрогены, следует максимально ограничить при наличии в анамнезе тромботического поражения вен.
Наиболее сложной представляется задача предотвращения ВТЭО у больных с генетически обусловленными тромбофилическими состояниями. Задачей, стоящей на повестке дня, следует считать биохимический скрининг таких нарушений. При перенесенном венозном тромбозе у пациентов с некоторыми тромбофилиями (например, дефицит AT-III), возможно, оправдано пожизненное применение наименее токсичных кумаринов (варфарина).
В заключение коснемся экономической стороны проблемы ВТЭО. Антикоагулянтную профилактику многие считают неоправданно дорогой. Действительно, стоимость Клексана на стандартный профилактический курс составляет около 52 долларов США. Однако стоимость лишь консервативного лечения флеботромбоза (не менее 300 долларов), а тем более тромбоэмболии легочных артерий (более 900 долларов), превышает таковую во много раз, даже если не рассматривать затраты на лечение хронической венозной недостаточности в отдаленном посттромботическом периоде. Целенаправленная профилактика ВТЭО позволяет не только сохранить жизнь и здоровье многих тысяч пациентов, но и значительные бюджетные средства российского здравоохранения.